CAR-T nei linfomi non-Hodgkin: una sfida terapeutica e organizzativa
Armando Santoro, Chiara De Philippis
Ematologia, Humanitas Cancer Center, Humanitas Clinical and Research Hospital, IRCCS Rozzano (MI)
L’introduzione delle CAR-T nel trattamento dei linfomi non-Hodgkin a grandi cellule B ricaduti e della leucemia linfoblastica B del giovane adulto in ricaduta rappresentano, probabilmente, una rivoluzione epocale nel trattamento di queste due malattie. Anche i risultati del trattamento con CAR-T in altre patologie ematologiche, come la leucemia linfatica cronica e il mieloma multiplo, sono molto promettenti, anche se ancora non così maturi. Sin dalla presentazione dei primi dati nei linfomi non-Hodgkin a grandi cellule B pluritrattati, vi è stato nel mondo onco-ematologico grande entusiasmo nel vedere le curve di sopravvivenza globale e soprattutto libera da progressione neppure immaginabili con gli approcci standard/sperimentali precedentemente disponibili. I dati iniziali sono stati successivamente confermati da vari studi condotti con tre differenti prodotti CAR-T (Tabella 1).
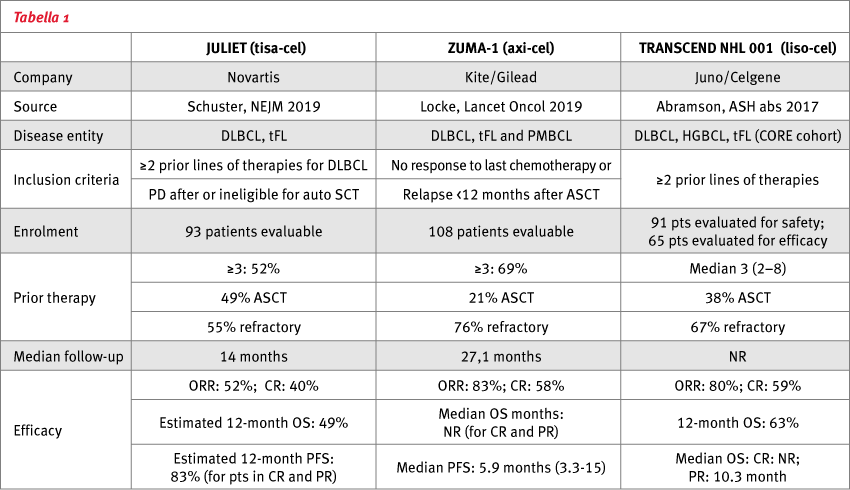
Complessivamente, si evidenzia un’altissima percentuale di risposte, con una quota di remissione completa compresa fra il 40 e il 60% e una sopravvivenza mediana superiore ai 12 mesi. Tali risultati sono stati ottenuti in una popolazione pesantemente pretrattata e senza reali opzioni terapeutiche alternative.
Anche l’alert legato alla tossicità (prevalentemente sindrome da rilascio delle citochine - CRS e tossicità neurologica) è andato sempre più riducendosi, grazie al riconoscimento tempestivo di tali eventi avversi, all’impiego di farmaci specifici come il tocilizumab e a una migliore selezione dei pazienti.
Questi dati sono stati confermati anche in una casistica “real world” su 134 pazienti, di cui circa la metà non rispettava i criteri di inclusione dello studio clinico con lo stesso farmaco (Tabella 2).
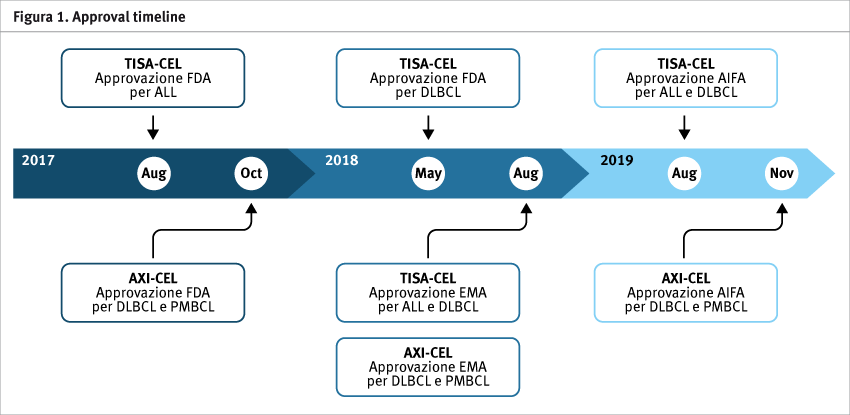
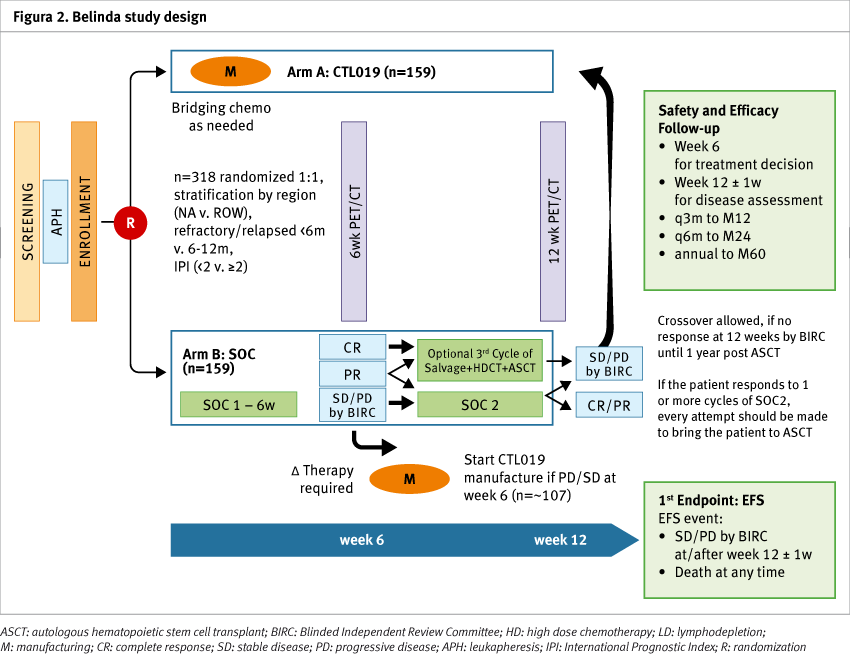
Sulla base di tali dati è arrivata l’approvazione da parte di AIFA di due prodotti CAR-T con differenti indicazioni (Figura 1). Inoltre, è già attivo in Italia uno studio di fase 3 (Belinda, Figura 2) che confronta, nei linfomi non Hodgkin a grandi cellule B o refrattari o ricaduti entro 12 mesi dal termine della terapia di prima linea, l’approccio classico di chemioterapia di induzione seguita, nei responsivi, da reinfusione di cellule staminali autologhe o da CAR-T (Tabella 3).
Il Cancer Center di Humanitas è al momento uno dei pochi centri autorizzato a eseguire trattamento con le cellule CAR-T in Italia.
L’iter approvativo è stato lungo e composto da varie fasi:
- prima di tutto abbiamo intrapreso un percorso, durato due anni, con le aziende (Novartis, Gilead e Celgene), al termine del quale siamo stati qualificati come centro accreditato;
- abbiamo quindi attivato una CAR-T Unit, coordinata dalla dott.ssa Stefania Bramanti con cui collabora attivamente la dott.ssa Chiara De Philippis, che include un gruppo di medici di varie specialità che collaborano attivamente al programma.
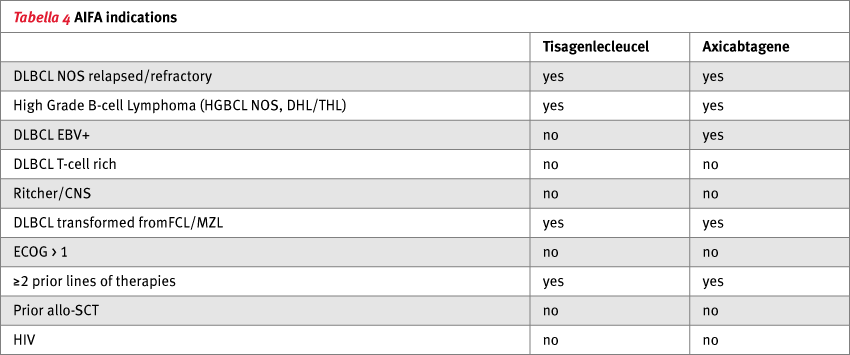
Il primo paziente è stato trattato il 4 novembre 2019 nell’ambito del protocollo compassionevole che forniva la Gilead per il trattamento dei linfomi primitivi del mediastino refrattari; da allora abbiamo trattato una serie di pazienti sia secondo le indicazioni approvate da AIFA (Tabella 4), sia nell’ambito dello studio clinico Belinda (chemio/auto vs CAR-T) già attivo presso il nostro centro, osservando dei risultati terapeutici sovrapponibili a quelli della letteratura, ma con un dato di tossicità nettamente minore.
Non abbiamo infatti riscontrato tossicità letali, ma solo lievi, e tutte sono state gestite in reparto, tranne un passaggio velocissimo in terapia intensiva di una paziente. Questo risultato è sicuramente correlato al trattamento precoce della CRS con il tocilizumab, come indicato dalle attuali linee guida. Inoltre, non abbiamo mai riscontrato neurotossicità, probabilmente per una selezione ottimale dei pazienti.
Una criticità riscontrata nei casi trattati, ma già riportata in letteratura, è il contenimento della malattia nel tempo che intercorre tra l’aferesi e la reinfusione, che è di circa 40 giorni. Questo lasso di tempo obbliga spesso all’impiego di una chemioterapia di “contenimento” per evitare una rapida evolutività della malattia in questo sottogruppo di pazienti a cattiva prognosi.
La terapia con CAR-T rimane comunque un approccio complesso che richiede un’organizzazione multidisciplinare, con un’area di degenza e del personale dedicato. Sarà quindi difficile pensare che tale procedura possa essere estesa a tutte le strutture ematologiche, anche se ovviamente il numero di quelle autorizzate è destinato ad aumentare.
Non si può inoltre non tenere conto dell’impatto economico di tale procedura, che è sicuramente elevato. Tuttavia, in Italia è stato ottenuto un meccanismo di “pay-by-results”, che tiene conto dei risultati a medio termine, che consentirà di contenere l’impatto economico. Da parte dei medici che lavorano presso i centri abilitati all’impiego delle CAR-T è indispensabile un impegno particolare nella selezione dei pazienti candidabili a tale procedura, nell’ottica di ottimizzare i risultati terapeutici, riducendo tossicità e costi inutili.
Un altro punto molto importante in questo periodo è quanto la pandemia COVID19 possa influenzare la selezione di pazienti e l’esecuzione della procedura terapeutica. Seppure l’intero sistema sanitario nazionale sia fortemente messo alla prova da questa emergenza mondiale, siamo in condizioni di garantire la terapia in maniera sicura e rispettando la tempistica, grazie alla presenza di un team dedicato e di un percorso COVID19-free che abbiamo attivato.
Considerando che la preparazione delle CAR-T avviene presso laboratori situati in USA e Germania, bisogna però segnalare la possibilità che si verifichino ritardi dei trasporti, secondari alla situazione contingente.