Introduzione
Il CD7 rappresenta un bersaglio promettente per la terapia con cellule T con recettore antigenico chimerico (CAR-T) nella leucemia linfatica acuta (LLA) a cellule T recidivata o refrattaria (R/R). Sul New England Journal of Medicine sono stati presentati i risultati di uno studio di fase 1 con cellule CAR anti-CD7 base-edited (BE-CAR7). Le cellule, prodotte mediante editing con tecnica CRISPR da C a T su cellule T da donatore, non richiedono la compatibilità con i riceventi.
Metodi
Nello studio di fase 1, le cellule BE-CAR7 sono state somministrate a 9 bambini (≤16 anni) con LLA a cellule T R/R e a 2 adulti trattati in regime di uso compassionevole. La linfodeplezione veniva effettuata con fludarabina, ciclofosfamide e alemtuzumab. I pazienti che risultavano in remissione al giorno 28 dopo l’infusione di BE-CAR7 procedevano a trapianto allogenico di cellule staminali ematopoietiche. L’endpoint primario era la sicurezza. Gli endpoints secondari includevano la durata della remissione, la sopravvivenza libera da malattia (DFS) e la sopravvivenza globale (OS).
Risultati
Le cellule BE-CAR7 sono state somministrate a 11 pazienti (9 bambini + 2 adulti). La linfodeplezione e le infusioni di BE-CAR7 non hanno determinato eventi avversi (EA) inaccettabili e cellule CAR7 circolanti sono state rilevate in tutti i pazienti. Per quanto riguarda l’endpoint primario di sicurezza, le complicanze includevano sindrome da rilascio di citochine di grado 1–4, rash transitori, citopenia multilineare e infezioni opportunistiche. Per quanto riguarda gli endpoints di efficacia, tutti i pazienti hanno ottenuto una remissione morfologica completa, con recupero incompleto della crasi ematica al giorno 28. Nove pazienti (82%) hanno ottenuto una remissione profonda (valutata mediante citometria a flusso o reazione a catena della polimerasi, PCR) e sono stati sottoposti a trapianto allogenico; i 2 pazienti con malattia minima residua (MRD) quantificabile nel midollo hanno ricevuto cure palliative (Figura 1).
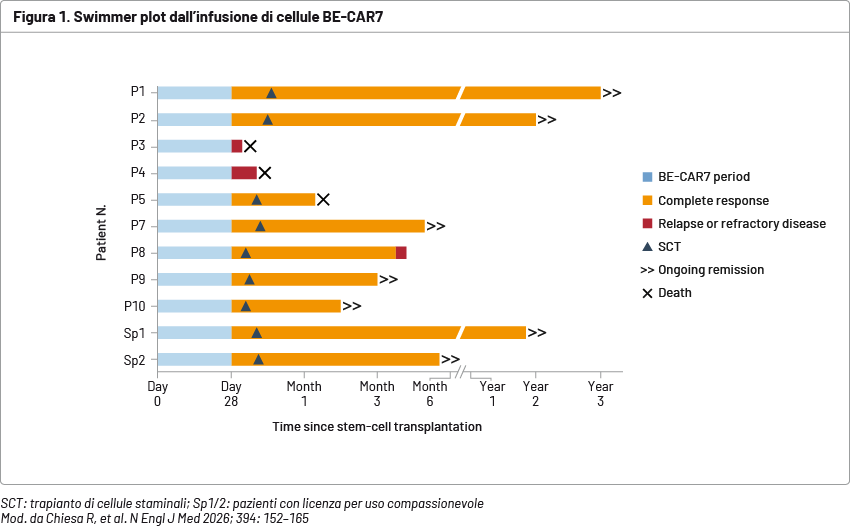
Nei pazienti sottoposti a trapianto è stata ottenuta una ricostituzione multilineare da donatore; le cellule BE-CAR7 sono state eliminate. Complessivamente, 7 degli 11 pazienti (64%) sono rimasti in remissione continuativa da 3 a 36 mesi dopo il trapianto; in 2 pazienti è stata riscontrata una recidiva leucemica con perdita dell’espressione di CD7. Nel post-trapianto, le riattivazioni virali sono state frequenti, con complicanze clinicamente significative correlate a infezioni virali in 3 pazienti.
Conclusioni
Le cellule BE-CAR7 universali hanno indotto remissione leucemica nei pazienti con LLA a cellule T R/R, consentendo un trapianto allogenico di cellule staminali ematopoietiche con esito favorevole nella maggior parte dei pazienti. Tra le limitazioni di questo approccio ci sono la perdita dell’antigene CD7 e il rischio di complicanze virali. Le BE-CAR7 rappresentano un promettente bridge off-the-shelf al trapianto allogenico. (Finanziato dal Medical Research Council e altri; ISRCTN15323014).