Introduzione
Ibrutinib, un inibitore della tirosin-chinasi di Bruton (BTKi), prolunga la sopravvivenza libera da progressione (PFS) se aggiunto all'immunochemioterapia (ICT) come trattamento di prima linea. Lo studio ENRICH ha confrontato la combinazione senza chemioterapia di ibrutinib e l'anticorpo anti-CD20 rituximab (ibrutinib–rituximab, IR) con l'ICT standard (rituximab–ciclofosfamide, doxorubicina, vincristina e prednisolone [R-CHOP]) o bendamustina–rituximab (BR) in pazienti di età pari o superiore a 60 anni affetti da linfoma mantellare (MCL) non trattato.
Metodi
Questo studio di superiorità di fase 2/3, randomizzato e in aperto, è stato condotto in 66 centri in Regno Unito, Svezia, Norvegia, Finlandia e Danimarca. Pazienti di età pari o superiore a 60 anni con MCL non trattato (stadio II-IV di Ann-Arbor, punteggio di performance status dell'Eastern Cooperative Oncology Group [ECOG PS] pari a 0–2) sono stati assegnati in modo casuale a ricevere rituximab più ICT o IR in un rapporto 1:1, stratificati in base alla scelta dell'ICT da parte dello sperimentatore. I pazienti assegnati in modo casuale al gruppo IR (intervento) hanno ricevuto 560 mg di ibrutinib orale al giorno in combinazione con 6–8 cicli di rituximab endovenoso da 375 mg/m2 il giorno 1 di ogni ciclo, secondo lo schema corrispondente alla scelta pre-randomizzazione dell'ICT (ogni 21 giorni per R-CHOP o ogni 28 giorni per BR). R-CHOP comprendeva 750 mg/m2 di ciclofosfamide, 50 mg/m2 di doxorubicina e 1,4 mg/m2 di vincristina il giorno 1 di ogni ciclo di 21 giorni, con 100 mg di prednisolone nei giorni 1–5 di ogni ciclo. BR comprendeva 90 mg/m² di bendamustina nei giorni 1 e 2 di ogni ciclo, in combinazione con 375 mg/m² di rituximab il giorno 1 di ogni ciclo. Tutti i pazienti responder in entrambi i gruppi al termine dell'induzione hanno ricevuto rituximab di mantenimento, somministrato ogni 8 settimane per 2 anni, mentre i pazienti assegnati al gruppo di intervento hanno continuato la terapia con ibrutinib fino alla progressione della malattia o a tossicità inaccettabile. L'esito primario era la PFS valutata dallo sperimentatore, stratificata in base alla scelta dell'ICT e analizzata nella popolazione intention-to-treat (ITT). Lo studio è stato registrato con numero EudraCT (2015–000832–13) ed è chiuso per il reclutamento.
Risultati
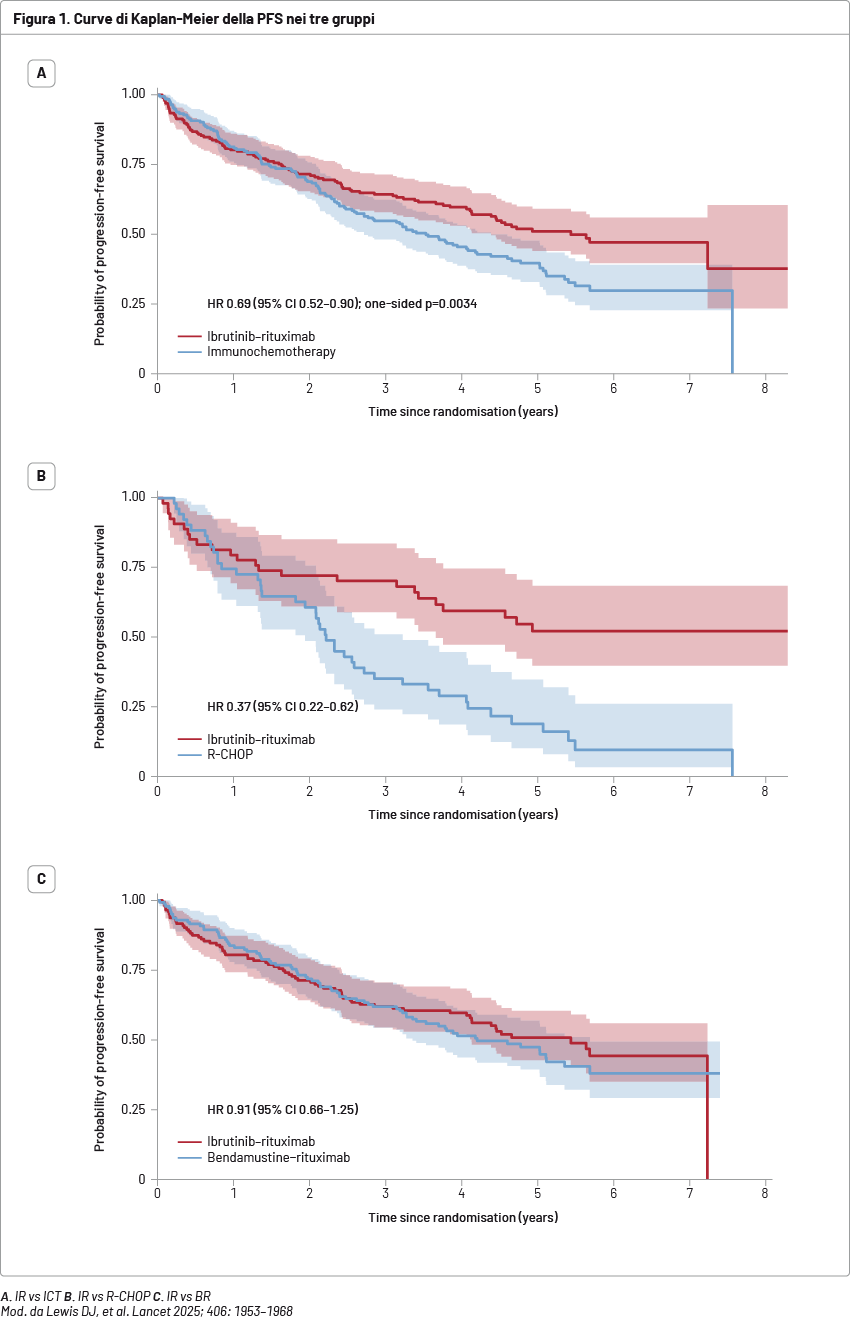
Tra il 15 febbraio 2016 e il 30 giugno 2021, 397 pazienti sono stati assegnati in modo casuale a ICT (controllo) o IR (intervento). Dei 397, 107 (27%) sono stati pre-assegnati all'ICT scelta R-CHOP e 290 (73%) sono stati pre-assegnati a ricevere BR. In totale, 198 sono stati assegnati al gruppo di controllo (53 a R-CHOP e 145 a BR) e 199 sono stati assegnati al gruppo di intervento. L'età mediana era di 74 anni (interquartile range, IQR 70–77) per il gruppo di intervento e di 74 anni (70–78) per il gruppo di controllo. Tra i pazienti, 296 (75%) erano di sesso maschile e 101 (25%) di sesso femminile; i dati etnici non sono stati raccolti. A un follow-up mediano di 47,9 mesi, la PFS mediana di IR è stata superiore all'ICT, con un hazard ratio (HR) aggiustato di 0,69 (confidence interval, CI 95%: 0,52–0,90); p=0,0034) (Figura 1A). Per i pazienti trattati con R-CHOP di scelta pre-randomizzazione, l'HR è stato pari a 0,37 (0,22–0,62) e per i pazienti trattati con BR, l'HR è stato pari a 0,91 (0,66–1,25) (Figura 1B-C).
Tra induzione e mantenimento, il 67% dei pazienti assegnati a IR e il 70% dei pazienti sottoposti a immunoterapia hanno riportato eventi avversi di grado 3 o superiore.
Conclusioni
Gli autori affermano che, a loro conoscenza, questo è il primo studio randomizzato sul MCL non trattato che dimostra un miglioramento significativo della PFS con IR rispetto all'ICT. Questo studio suggerisce che la terapia IR dovrebbe essere considerata un nuovo standard di cura per il trattamento di prima linea dei pazienti anziani con MCL.