Introduzione
Dasatinib è un trattamento efficace per la leucemia acuta Philadelphia-positiva (Ph+), ma alcuni pazienti sviluppano resistenza. Asciminib si distingue per un meccanismo d’azione differente: non si lega al dominio chinasico di BCR::ABL1 ma al sito miristoilico, è stato ideato per essere selettivo e privo di effetti collaterali off-target, oltre che per poter essere utilizzato in combinazione con gli altri farmaci. É efficace nei pazienti con mutazioni, inclusa la T315I. Il farmaco agisce mimando l’azione di un peptide miristoilico ad azione inibitoria sull’attività di ABL, perso durante la traslocazione t(9;22); l’azione del farmaco permette, quindi, l’inibizione allosterica sull’attività chinasica di BCR-ABL1, ripristinando così l'autoinibizione della chinasi ABL1 che viene persa a seguito della traslocazione genica di BCR::ABL1. La combinazione di dasatinib con asciminib, un inibitore allosterico di BCR::ABL1, potrebbe consentire l’ottenimento di risposte profonde e prevenire l'emergere di cloni resistenti a dasatinib.
Metodi
Nello studio di fase 1, 24 adulti con leucemia linfoblastica acuta (ALL) Ph+ (ALL, n = 22; p190, n=16; p210, n=6) e leucemia mieloide cronica (LMC) in crisi blastica linfoide (n=2) sono stati trattati con dosi giornaliere crescenti di asciminib in combinazione con dasatinib 140 mg/die + prednisone 60 mg/m²/die, per determinare la dose massima tollerata. Dopo un'induzione di 28 giorni, dasatinib e asciminib venivano proseguiti indefinitamente o fino al trapianto di cellule staminali ematopoietiche.
Risultati
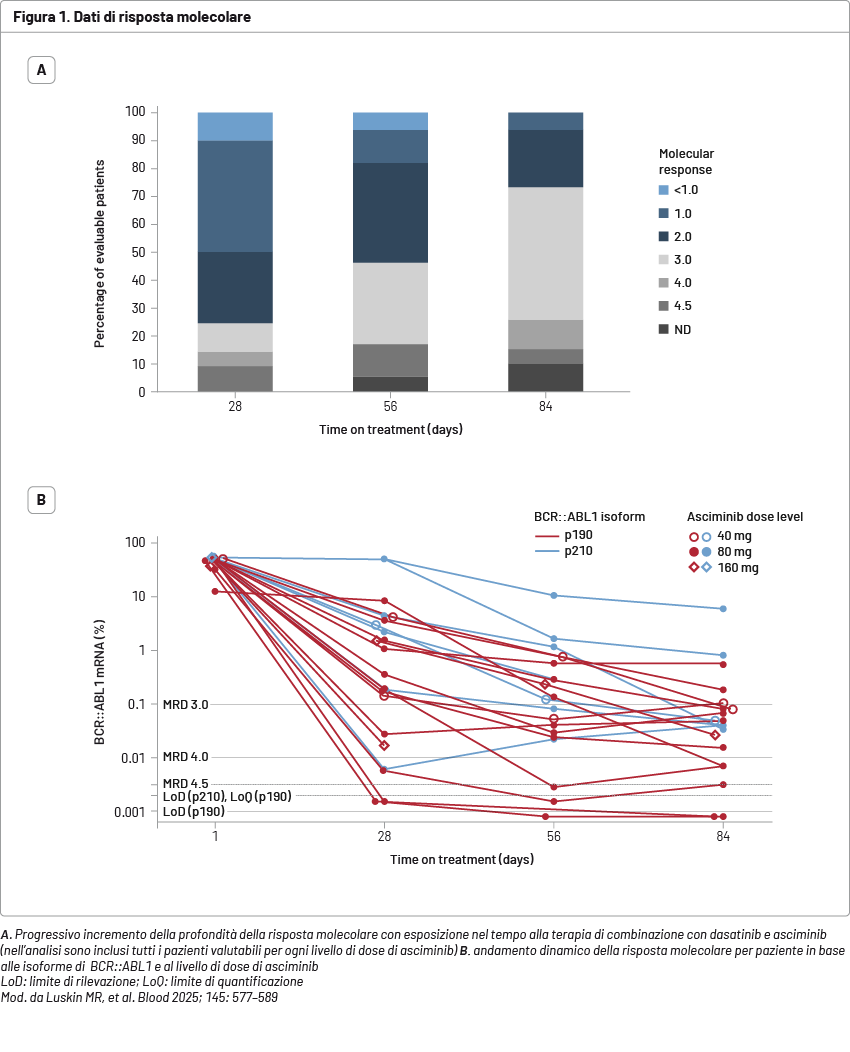
L'età mediana dei pazienti era di 64,5 anni (33–85 anni; 50% avevano un età ≥65 anni). La dose raccomandata per la fase 2 di asciminib è stata di 80 mg al giorno. La tossicità limitante la dose a 160 mg al giorno è stata un aumento asintomatico di grado 3 degli enzimi pancreatici, senza pancreatite sintomatica. Non si sono verificati eventi vaso-occlusivi. Tra i pazienti con ALL de novo, i tassi di remissione ematologica completa ai giorni 28 e 84 sono stati dell’84 e del 100%, rispettivamente. Al giorno 84, il 100% dei pazienti ha ottenuto la remissione citogenetica completa, l’89% ha raggiunto la negatività per la malattia residua misurabile (MRD, <0,01%) tramite citometria a flusso e il 74 e il 26% hanno raggiunto un livello di BCR::ABL1 inferiore a 0,1 e 0,01%, rispettivamente, mediante reazione a catena della polimerasi inversa quantitativa (RT-qPCR) (Figura 1).
Conclusioni
L’inibizione duale di BCR::ABL1 con dasatinib e asciminib è sicura e mostra un'efficacia promettente come terapia nei pazienti con ALL Ph+ de novo. Lo studio pone le basi per la progettazione di futuri studi sulla ALL Ph+, nei quali un terzo agente mirato venga aggiunto alla combinazione classica di inibitori della tirosin-chinasi e blinatumomab come terapia di induzione. Inoltre, sebbene questo studio sia stato concepito esclusivamente come un trial di induzione, asciminib dovrebbe essere esplorato anche come componente dei regimi post-remissione. Questo studio è stato registrato su ClinicalTrials.gov (NCT02081378).