Introduzione
Lo studio AMPLIFY ha recentemente stabilito che acalabrutinib-venetoclax-obinutuzumab (AVO) a durata fissa costituisce una nuova opzione di cura standard per i pazienti con leucemia linfatica cronica (LLC) non trattata in precedenza con TP53 wild type (WT); tuttavia, a causa del braccio di controllo della chemioimmunoterapia, AMPLIFY ha escluso i pazienti con aberrazione di TP53 ad alto rischio, per i quali gli standard di cura attuali sono la terapia continua con inibitori della tirosin-chinasi di Bruton (BTKi) o, in alternativa, doppiette a base di venetoclax a durata fissa. AVO non è stato precedentemente valutato nei pazienti con LLC e aberrazione di TP53.
Metodi
Questo studio di fase 2, multicentrico, sponsorizzato, ha arruolato pazienti con LLC ad alto rischio (per la presenza di aberrazioni di TP53) naïve al trattamento (numero ClinicalTrials.gov, NCT03580928). I pazienti hanno ricevuto acalabrutinib, obinutuzumab e poi venetoclax secondo lo schema AVO dello studio AMPLIFY (che abbiamo presentato nel secondo numero del 2024, ndr), con uno schema sequenziale e di combinazione e con una durata guidata dalla malattia residua misurabile (MRD). I pazienti che avevano raggiunto una MRD non rilevabile (uMRD) dopo 15 o 24 cicli potevano interrompere il trattamento. L'endpoint primario era la risposta completa (CR) con uMRD del midollo osseo (BM-uMRD) all'inizio del ciclo 16.
Risultati
Sono stati arruolati 72 pazienti, inclusi 45 pazienti con aberrazione di TP53. I tassi di CR con BM-uMRD all'inizio del ciclo 16 erano del 42% nei pazienti con aberrazione di TP53 e del 42% in tutti i partecipanti, mentre i tassi di BM-uMRD erano del 71 e del 78%, rispettivamente. Le tossicità ematologiche erano principalmente di basso grado, con tossicità cardiovascolari e complicazioni emorragiche poco frequenti. Dopo un follow-up mediano di 55,2 mesi, 10 pazienti erano progrediti, inclusi 4 con trasformazione, e 3 pazienti erano deceduti. La sopravvivenza libera da progressione a 4 anni e la sopravvivenza globale per i pazienti con o senza aberrazione di TP53 erano del 70/96% e dell'88/100%, rispettivamente (Figura 1).
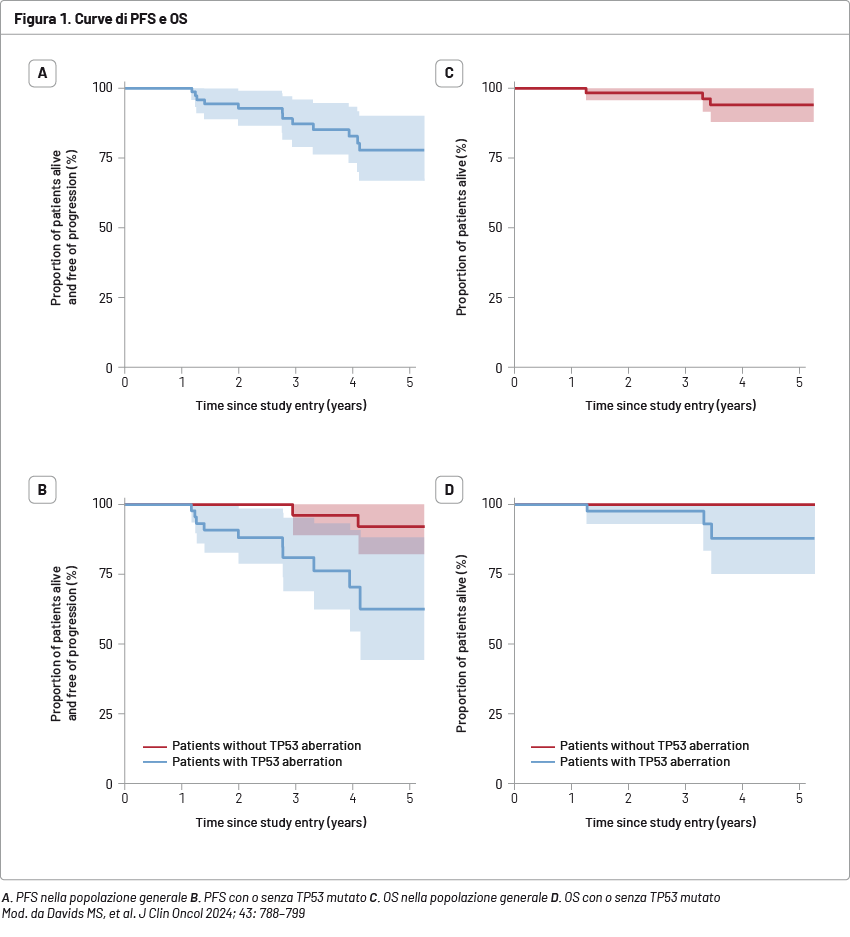
Conclusioni
L'AVO è risultato altamente attivo e ben tollerato nei pazienti con LLC ad alto rischio non precedentemente trattata, supportandone l'uso come nuova opzione di trattamento standard.