Numero speciale di "Impact Factor News” n° 4 - Ottobre 2018
Introduzione
Rituximab associato a chemioterapia rappresenta oggi lo standard di trattamento in prima linea nei pazienti affetti da linfoma follicolare (FL) con high tumor burden. Nonostante questo trattamento combinato sia altamente efficace, circa la metà dei pazienti va incontro a recidiva di malattia. Questo ha portato nel corso degli anni a testare terapie che avessero come obiettivo quello di ridurre le tossicità nell’ipotesi di dover ritrattare più volte nel tempo i pazienti affetti da tale patologia. Lenalidomide ha dimostrato un’attività promettente nei linfomi indolenti B in associazione a rituximab. Nel 2016 Fowler e colleghi hanno pubblicato i risultati di uno studio di fase II in pazienti affetti da FL in prima linea con lo schema chemo-free rituximab-lenalidomide dimostrando l’alta tollerabilità associata a risposte molto promettenti. Lo studio però aveva visto l’arruolamento di pazienti con malattia avanzata ma che necessitavano di una terapia, secondo i criteri GELF, solo in una minoranza di casi.
Metodi
In questo lavoro gli Autori hanno riportato i risultati di uno studio prospettico multicentrico, di fase 3 di superiorità per valutare l’associazione rituximab-lenalidomide versus lo standard immunochemioterapico in pazienti affetti da FL high tumor burden in prima linea.
I pazienti venivano assegnati attraverso una randomizzazione a ricevere uno dei due regimi di trattamento, seguiti entrambi da mantenimento con rituximab. Lo schema rituximab-lenalidomide consisteva nella somministrazione dei due farmaci in 18 cicli seguiti dallo schema classico di mantenimento con rituximab ogni 8 settimane per 12 dosi (6 dosi aggiuntive). Lo schema rituximab-chemioterapia consisteva nell’associazione all’anticorpo monoclonale anti-CD20 dello schema chemioterapico considerato lo standard presso ciascun centro partecipante, seguita dallo schema classico di mantenimento con rituximab ogni 8 settimane per 12 dosi (12 dosi aggiuntive). Gli obiettivi primari dello studio erano: il numero di risposte complete e la sopravvivenza libera da malattia a 120 settimane dalla fine dell’induzione. (Studio sponsorizzato da Celgene; Studio RELEVANCE registrato su ClinicalTrials.gov numeri: NCT01476787 e NCT01650701, e EudraCT numero: 2011-002792-42.)
Risultati
Nello studio sono stati inclusi e randomizzati 1030 pazienti: 513 pazienti nel braccio rituximab-lenalidomide, 517 pazienti nel braccio rituximab-chemioterapia. La percentuale di remissioni complete confermate e non confermate a 120 settimane è stata del 48% (95% CI, 44–53) nel gruppo rituximab-lenalidomide e del 53% (95% CI, 49–57) nel gruppo rituximab-chemioterapia (p=0,13) (Tabella 1).
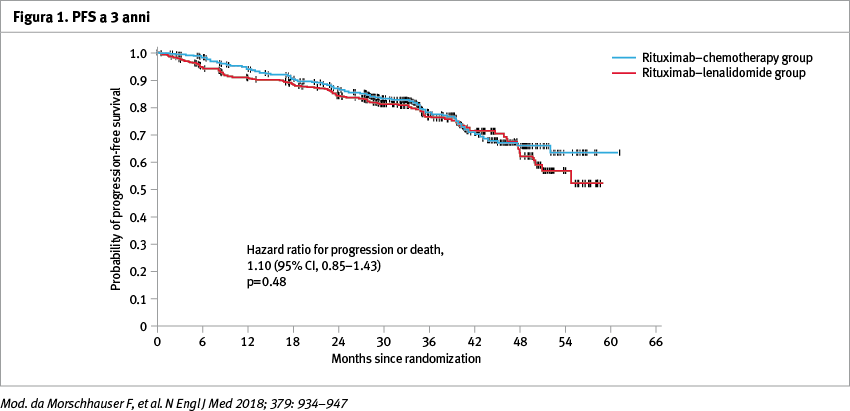
A tre anni la sopravvivenza libera da malattia è stata del 77% (95% CI, 72–80) nel gruppo rituximab-lenalidomide e del 78% (95% CI, 74–82) nel gruppo rituximab-chemioterapia, rispettivamente (Figura 1).
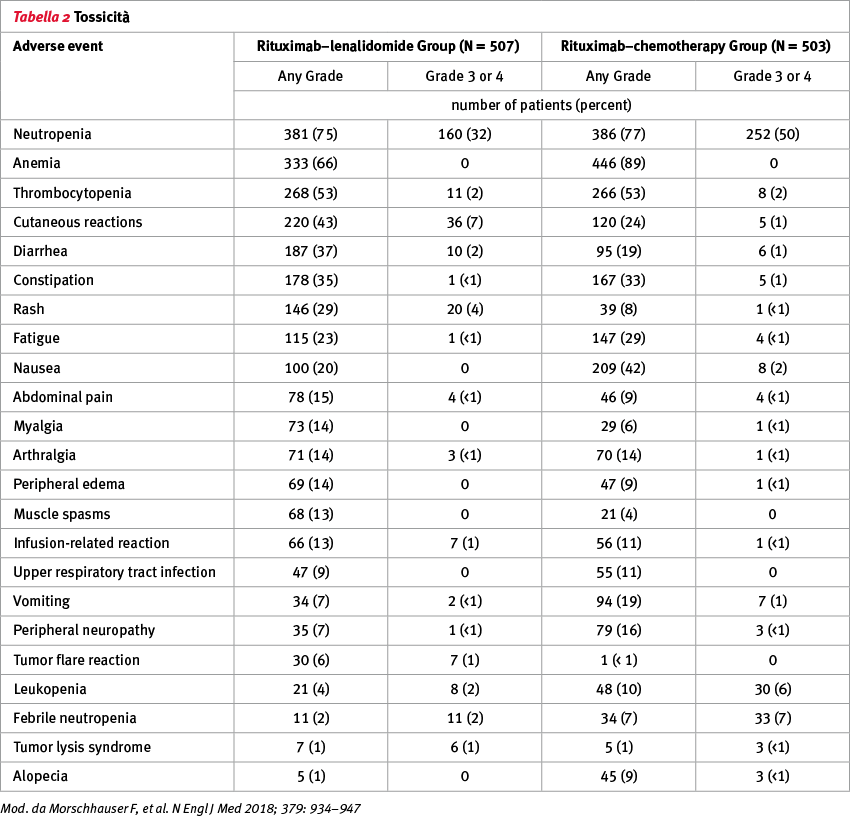
Per quanto concerne le tossicità, la percentuale di neutropenia severa (grado 3 o 4) è stata 32% nel gruppo rituximab-lenalidomide versus 50% nel gruppo rituximab-chemioterapia, la percentuale di neutropenia febbrile del 2 versus 7%. La percentuale di reazioni cutanee di grado severo (grado 3 o 4) è stata del 7% nel gruppo rituximab-lenalidomide versus l’1% nel gruppo rituximab-chemioterapia (Tabella 2).
Conclusioni
Al fine di poter registrare lo schema in prima linea il disegno dello studio era basato sull’ipotesi di superiorità dello schema chemo-free sul trattamento standard di abbinamento chemio-immunoterapia. Gli Autori concludono che l’obiettivo è stato fallito, dal momento che i due approcci hanno dimostrato pari efficacia. Ma se da un punto prettamente statistico lo studio va definito come negativo, dal punto di vista pratico i dati ottenuti confermano che lenalidomide associata a rituximab sia in grado di ottenere delle remissioni complete che si traducono a due anni in una sopravvivenza libera da malattia comparabile a quella ottenuta con schemi di chemioterapia standard. Le differenze in termini di tossicità osservate nei due gruppi di trattamento aprono nuovi scenari per una terapia sempre più personalizzata.
Una riflessione merita il disegno dello studio che è stato quello di stabilire nell’ipotesi iniziale, poi mantenuta nel trial, di effettuare uno studio di superiorità e che ha portato quindi al fallimento dell’obiettivo, dal momento che lo schema chemo-free si è dimostrato pari a quello di combinazione anticorpo monoclonale-chemioterapia. Per uno studio di non inferiorità il campione avrebbe dovuto essere di 1300 pazienti versus i 1030 di quello di superiorità. Lo scarto numerico non è così ampio ed evidentemente sottolinea come gli Sperimentatori fossero certi a priori che l’associazione chemo-free fosse superiore al trattamento standard. Purtroppo la conseguenza negativa è sicuramente maggiore, dal momento che la negatività dello studio non può portare alla registrazione dello schema in prima linea nonostante la chiara efficacia.