Numero speciale di "Impact Factor News” n° 1 - Aprile 2017
Background
Il blinatumomab è un anticorpo bispecifico che, legandosi contemporaneamente ai linfociti T citotossici CD3 positivi e ai i blasti Cd19+ della leucemia linfoblastica acuta (ALL), consente il riconoscimento e la distruzione delle cellule leucemiche da parte dei linfociti del paziente. Ne è stato approvato l’uso nelle leucemia linfoblastica acuta a precursori B recidivata/refrattaria sulla base di un singolo trial di fase 2 che ne evidenziava l’efficacia e la sicurezza d’impiego (Topp MS, et al. Lancet Oncol 2015; 16: 57).
Sul NEJM Kantarjian et al. hanno pubblicato i dati del trial di fase 3 che ha posto a confronto il monoclonale con la chemioterapia standard confermando il beneficio conferito dall’uso di blinatumomab in questo setting di pazienti in termini di event-free survival (EFS) e overall survival (OS).
Metodi
Lo studio multicentrico randomizzato di fase 3 ha arruolato 405 pazienti affetti da LLA pre-B pretrattati a ricevere blinatumomab o una chemioterapia standard a scelta dello sperimentatore con rapporto 2:1. L’obiettivo primario dello studio era la OS. Gli endpoints secondari includevano la remissione completa e l’endpoint combinato della remissione completa alla remissione completa con recupero ematologico parziale o incompleto.
Risultati
Dei 405 pazienti inclusi, 271 sono stati trattati nel braccio sperimentale con blinatumomab e 134 con chemioterapia standard, 376 pazienti hanno ricevuto almeno una dose del trattamento pianificato.
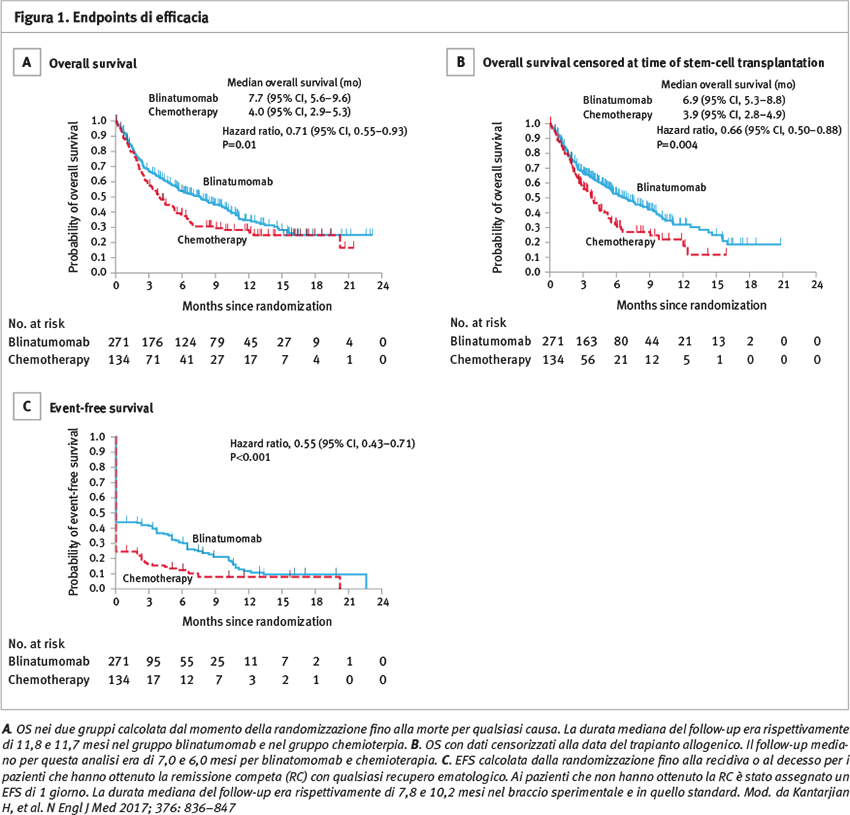
La OS è stata maggiore nel braccio blinatumomab rispetto al braccio di controllo con un OS mediana rispettivamente di 7,7 e 4 mesi (HR per rischio di morte 0,71, IC al 95%, 0,55–0,93; p = 0,01). Il beneficio di sopravvivenza è stato generalmente mantenuto in tutti i sottogruppi, indipendentemente dall’età, dalla pregressa terapia di salvataggio o dal pregresso trapianto allogenico di cellule staminali (alloSCT).
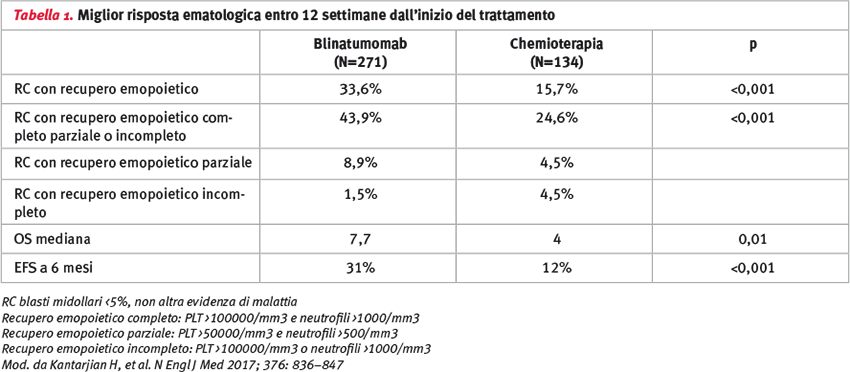
Come con la sopravvivenza, il tasso di remissione completa entro le 12 settimane dall’inizio del trattamento è stato maggiore nel braccio blinatumomab. In particolare il doppio dei pazienti ha raggiunto la remissione con recupero ematologico completo rispetto alla chemioterapia (Tabella 1).
Analogamente, nei pazienti che avevano ottenuto la risposta completa, la EFS è stata maggiore nel gruppo blinatumomab con un EFS stimata a 6 mesi del 31 vs 12% del gruppo standard (HR 0,55; IC al 95% 0,43–0,71; p <0,001), così come lo è stata la durata della risposta (durata mediana 7,3 vs 4,6 mesi).
In entrambi i gruppi il 24% dei pazienti è stato sottoposto a trapianto allogenico.
Eventi avversi di grado 3 sono stati registrati nell’87% dei pazienti trattati con blinatumomab e nel 92% dei pazienti sottoposti a chemioterapia. I tassi di eventi avversi fatali erano il 19 e il 17% nei gruppi blinatumomab e chemioterapia, rispettivamente. I tassi di interruzione del trattamento a causa di eventi avversi sono stati il 12% con blinatumomab e l'8% con la chemioterapia.
Conclusioni
Blinatumomab ha determinato un vantaggio significativo, non solo come il tasso di risposte ma anche in termini di sopravvivenza, rispetto alla chemioterpia in pazienti precedentemente sottoposti a farmaci mielo- e immuno-soppressori. Gli Autori considerano questo risultato interessante e auspicano che lo sviluppo di ulteriori strategie terapeutiche immunomediate possa ulteriormente migliorarne l’efficacia. (TOWER ClinicalTrials.gov number, NCT02013167.)