Numero speciale di "Impact Factor News” n° 1 - Aprile 2017
Obiettivi
Il potenziale beneficio della chemioterapia ad alte dosi nei pazienti affetti da DLBCL nel contesto della terapia di prima linea è ancora materia di dibattito a livello internazionale. In questo studio gli Autori hanno voluto saggiarne la reale efficacia disegnando un trial di fase 3, prospettico, di confronto tra il regime standard con rituximab associato a ciclofosfamide, doxorubicina, vincristina e prednisone (R-CHOP)-14 (per 8 cicli) e rituximab associato a chemioterapia sequenziale ad alte dosi con supporto di cellule staminali autologhe (R-HDS+ASCT).
Pazienti e metodi
Dal giugno 2005 al giugno 2011, 246 pazienti ad alto rischio secondo lo score prognostico internazionale IPI (high-risk 44% e high-intermediate 56%) sono stati assegnati in modo randomizzato a ricevere uno schema di prima linea con R-CHOP o con R-HDS+ASCT; di questi 235 erano idonei all’analisi in intention-to-treat. L’obiettivo primario di efficacia dello studio è stato identificato nella sopravvivenza libera da eventi a 3 anni (EFS a 3 anni). I risultati dello studio sono stati valutati sulla base di un’analisi di intention-to-treat.
Risultati
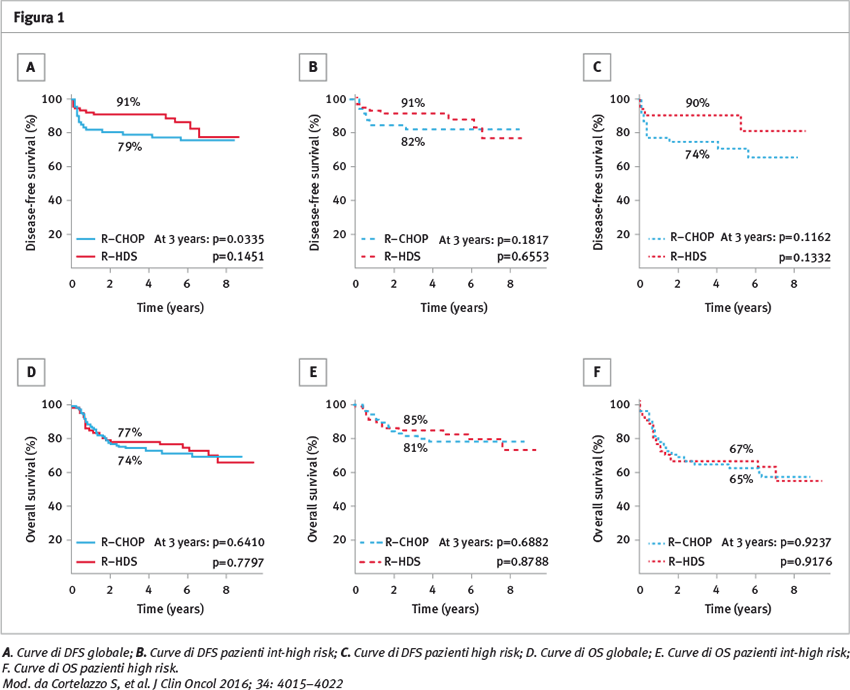
Per quanto concerne le risposte al termine di ciascun trattamento non vi è stata differenza tra i due bracci dello studio R-CHOP versus R-HDS+ASCT (risposte complete: 78 versus 76%; risposte parziali: 5 versus 9%), così come i fallimenti del trattamento sia in termini di non risposta: 15 versus 11%, sia di mortalità precoce legata al trattamento: 2 versus 3%. Dopo un follow-up mediano di più di 5 anni, la EFS a 3 anni è stata del 62 versus 65% (p=0,83). A 3 anni, il braccio delle R-HDS+ASCT rispetto a quello con R-CHOP presentava una migliore PFS (79 versus 91%, rispettivamente; p=0,034), ma questo vantaggio veniva perso a lungo termine con le morti tardive legate al trattamento.
Per i dati di sopravvivenza non sono state osservate differenze statisticamente significative sia in termini di PFS (65 versus 75%, rispettivamente; p=0,12), sia di OS (74 versus 77%, rispettivamente; p=0,64). Per i dati di tossicità si è invece registrata una differenza statisticamente significativa a sfavore del braccio R-HDS che ha presentato sia una tossicità ematologica maggiore (p=0,001) sia un numero di eventi infettivi superiore (p=0,001) alla terapia standard.
Conclusioni
Gli Autori affermano che in questo studio di prima linea la terapia con alte dosi sequenziali supportate da cellule staminali autologhe non ha apportato un miglioramento dell’outcome rispetto al trattamento standard nei pazienti affetti da linfoma diffuso a grandi cellule B ad alto rischio IPI.