Numero speciale di "Impact Factor News” n° 1 - Aprile 2020
Introduzione
Isatuximab è un anticorpo monoclonale che lega un epitopo specifico sul recettore CD38 umano e ha attività antitumorale attraverso molteplici meccanismi d'azione. In un precedente studio di fase 1b, circa il 65% dei pazienti con mieloma multiplo recidivante e refrattario ha ottenuto una risposta globale con una combinazione di isatuximab con pomalidomide e desametasone a basso dosaggio. Lo scopo di questo studio era di determinare il beneficio di sopravvivenza libera da progressione di isatuximab più pomalidomide e desametasone rispetto a pomalidomide e desametasone in pazienti con mieloma multiplo recidivante e refrattario.
Metodi
È stato condotto uno studio randomizzato, multicentrico, in aperto, di fase 3 in 102 ospedali in 24 paesi in Europa, Nord America e Asia-Pacifico. I partecipanti eleggibili erano pazienti adulti con mieloma multiplo recidivante e refrattario che avevano ricevuto almeno due precedenti linee di trattamento, tra cui lenalidomide e un inibitore del proteasoma. I pazienti sono stati esclusi se erano refrattari al precedente trattamento con un anticorpo monoclonale anti-CD38. I pazienti sono stati assegnati in modo casuale (1: 1) a isatuximab 10 mg/kg più pomalidomide 4 mg più desametasone 40 mg (20 mg per pazienti di età ≥75 anni) o pomalidomide 4 mg più desametasone 40 mg. La randomizzazione è stata effettuata utilizzando la tecnologia di risposta interattiva e stratificata in base al numero di precedenti linee di trattamento (2-3 vs >3) e all'età (<75 anni vs ≥75 anni). I trattamenti sono stati assegnati in base a uno schema di randomizzazione bloccato permutato con una dimensione di blocco di quattro. Il gruppo isatuximab-pomalidomide-desametasone ha ricevuto isatuximab per via endovenosa nei giorni 1, 8, 15 e 22 nel primo ciclo di 28 giorni, quindi nei giorni 1 e 15 nei cicli successivi. Entrambi i gruppi hanno ricevuto pomalidomide orale nei giorni da 1 a 21 in ciascun ciclo e desametasone orale o endovenoso nei giorni 1, 8, 15 e 22 di ciascun ciclo. Il trattamento è continuato fino alla progressione della malattia, alla tossicità inaccettabile o alla sospensione del consenso. Sono state consentite riduzioni della dose per reazioni avverse per pomalidomide e desametasone, ma non per isatuximab. L'endpoint primario era la progression-free survival (PFS), determinata da un comitato di risposta indipendente e valutata nella popolazione ITT. La sicurezza è stata valutata in tutti i partecipanti che hanno ricevuto almeno una dose del farmaco in studio. Questo studio è registrato presso ClinicalTrials.gov, NCT02990338.
Risultati
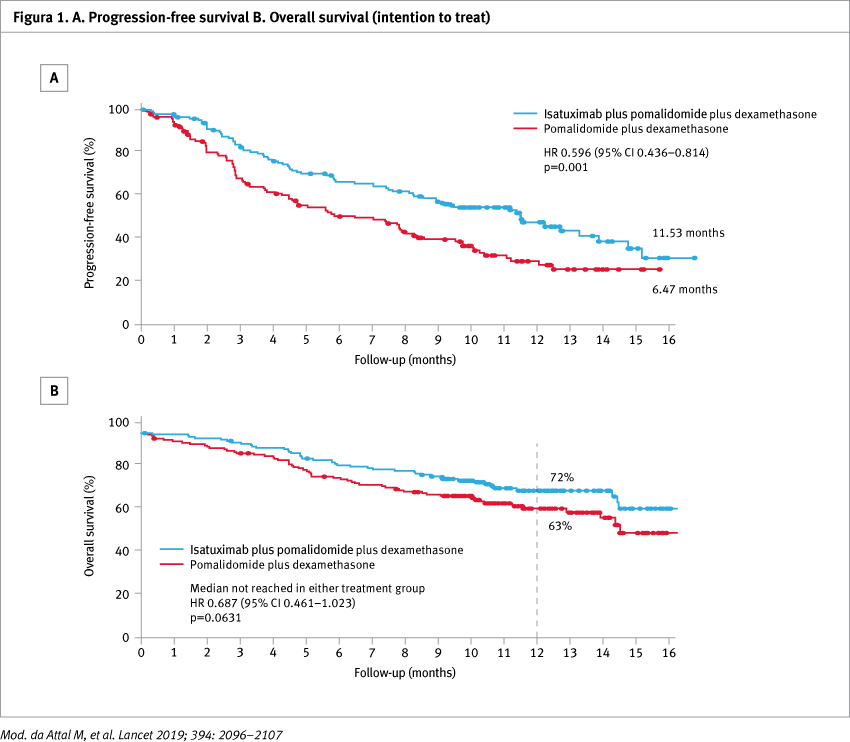
Tra gennaio 2017 e febbraio 2018, 307 pazienti sono stati randomizzati con rapporto 1:1, 154 nel braccio isatuximab-pomalidomide-desametasone e 153 nel braccio pomalidomide-desametasone. Con un follow-up mediano di 11,6 mesi (range 10,1–13,9), la PFS mediana è stata di 11,5 mesi (IC 95% 8,9–13,9) nei trattati con isatuximab-pomalidomide-desametasone contro 6,5 mesi (range 4,5–8,3) nel gruppo pomalidomide-desametasone (HR 0,596, IC 95% 0,44–0,81; p=0,001) (Figura 1).
Gli eventi avversi più frequenti di qualsiasi grado con isatuximab-pomalidomide-desametasone vs pomalidomide-desametasone sono state le reazioni da infusione (56 [38%] vs 0), le infezioni del tratto respiratorio superiore (43 [28%] vs 26 [17% ]) e la diarrea (39 [26%] contro 29 [20%]). Si sono verificati 12 eventi avversi con esito fatale (8%) nel gruppo isatuximab-pomalidomide-desametasone e 14 (9%) nel gruppo pomalidomide-desametasone. Un paziente (<1%) nel gruppo isatuximab-pomalidomide-desametasone (sepsi) e due pazienti (1%) nel gruppo pomalidomide-desametasone (polmonite e infezione del tratto urinario) sono deceduti per eventi avversi correlati al trattamento.
Conclusioni
Gli Autori concludono che l'aggiunta di isatuximab alla doppietta pomalidomide-desametasone migliora significativamente la PFS in pazienti con mieloma multiplo recidivante e refrattario. Isatuximab è un'importante nuova opzione di trattamento per la gestione del mieloma recidivato e refrattario, in particolare per i pazienti che diventano refrattari a lenalidomide e a un inibitore del proteasoma.