Numero speciale di "Impact Factor News” n° 4 - Ottobre 2021
Introduzione
Il 60% dei pazienti con leucemia mieloide acuta di nuova diagnosi (ND-AML) ottiene una risposta completa (CR) con la terapia di prima linea, ma il 30–40% dei pazienti recidiva. L’AML recidivata/refrattaria (R/R) rimane una popolazione a prognosi avversa con poche opzioni terapeutiche. Nei pazienti anziani l’aggiunta dell’inibitore di BCL-2 venetoclax ai trattamenti standard a bassa intensità (azacitidina, decitabina o basse dosi di citarabina) ha dato risultati soddisfacenti e si sta affermando come standard di cura. Sulla base di questi dati, DiNardo e colleghi hanno valutato la sicurezza e l'efficacia dell’aggiunta di venetoclax al trattamento con fludarabina, citarabina, G-CSF e idarubicina (FLAG-IDA) nei pazienti affetti da ND-AML e AML R/R e candidabili a terapia intensiva.
Metodi
Nella fase iniziale Ib (PIB) di questo studio di fase Ib/II, sono stati arruolati pazienti con AML R/R utilizzando un algoritmo di dose-escalation di 3 + 3 per l'identificazione della dose massima tollerata e delle tossicità limitanti la dose. Nella fase II sono stati arruolati i pazienti in due bracci, suddivisi in base allo stato di malattia, per valutare gli endpoints risposta e time-to event: fase IIa (PIIA) ND-AML e fase IIb (PIIB) AML R/R. La risposta era valutata come risposta completa composita (CRc) (risposta completa, CR + risposta completa con recupero ematologico incompleto, CRi + risposta completa con recupero ematologico parziale, CRh). Nell’overall response rate (ORR) sono stati compresi i pazienti in CRc, in remissioni morfologica (MLFS) e in risposta parziale (PR).
Risultati
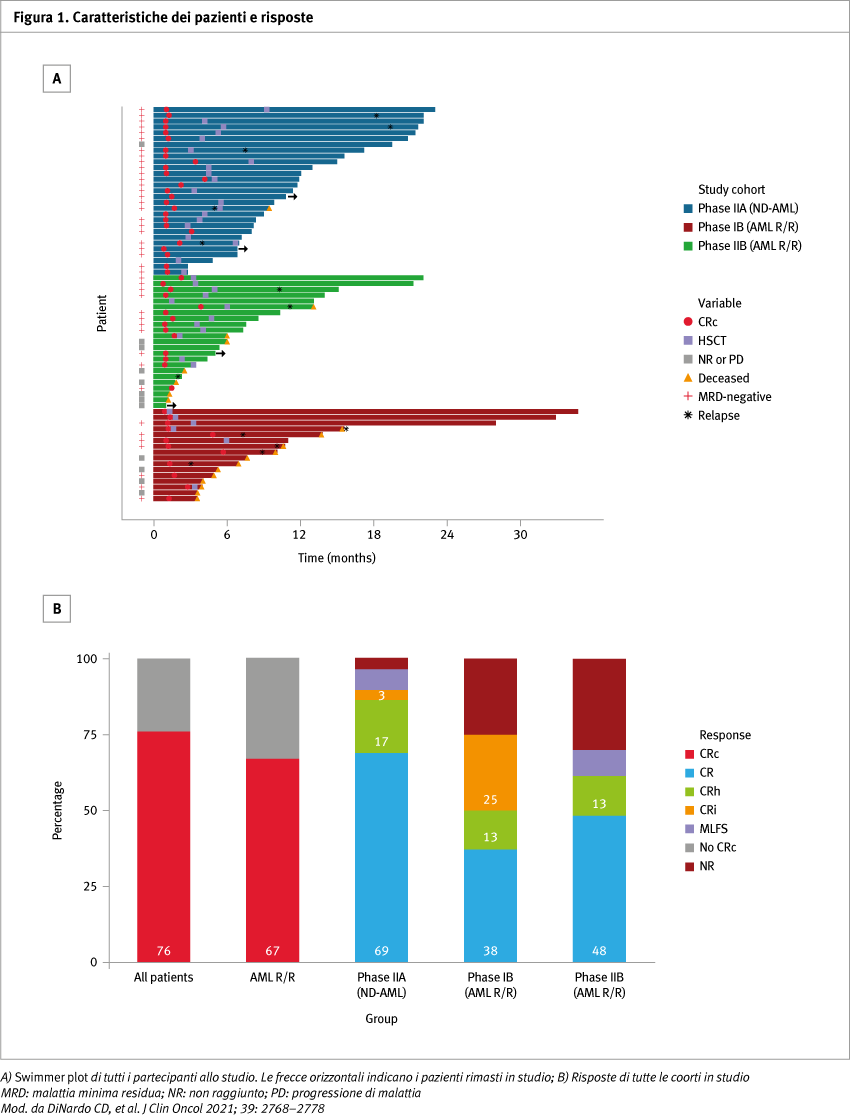
Lo studio ha arruolato 68 pazienti (PIB 16, PIIA 29, PIIB 23) con un’età media di 46 anni (range 20–73). Per quanto riguarda la tollerabilità del trattamento, gli eventi avversi di grado 3 e 4 verificatisi in ≥10% dei pazienti includevano neutropenia febbrile (50%), batteriemia (35%), polmonite (28%) e sepsi (12%). Le batteriemie sono state più frequenti nei pazienti con AML R/R (46 vs 21%). La combinazione FLAG-IDA + venetoclax ha determinato alti tassi di risposte, con un ORR nei gruppi PIB, PIIA e PIIB rispettivamente del 75, 97 e 70%; il tasso di CRc era del 75, 90 e 61%. Dei pazienti in CRc, il 96% con ND-AML e il 69% con AML R/R erano MRD-negativi. Dopo un follow-up mediano di 12 mesi, l’overall survival (OS) mediana per entrambe le coorti PII non è stata raggiunta. L’OS nei gruppi PIB, PIIA e PIIB era rispettivamente del 70, 94 e 68%. I pazienti inclusi hanno ricevuto un numero mediano di due cicli. Il motivo principale di interruzione del trattamento è stato il passaggio al trapianto di cellule staminali ematopoietiche (HSCT) allogenico, con il 56% dei pazienti trapiantati (ND-AML 69%, AML R/R 46%). Nell’AML R/R, l’HSCT allogenico ha determinato un miglioramento significativo dell’OS (OS mediana: non raggiunta; OS a un anno: 87%). La sopravvivenza a un anno post-HSCT è stata del 94% in ND-AML e del 78% in AML R/R.

Conclusioni
La combinazione FLAG-IDA + venetoclax è un regime intensivo caratterizzato da un profilo di tossicità prevedibile e accettabile nei pazienti sia con ND-LMA sia con AML R/R. Nonostante i limiti di uno studio condotto in un numero esiguo di pazienti e non randomizzato, gli alti tassi di risposte e di MRD negativa lo rendono un potenziale regime strategico come bridge al trapianto allogenico.


