Numero speciale di "Impact Factor News” n° 1 - Aprile 2020
Introduzione
Luspatercept è il capostipite di una classe di farmaci stimolanti l’eritropoiesi che si lega trasformando i ligandi della superfamiglia del fattore di crescita β per ridurre la segnalazione di SMAD2 e SMAD3, e contribuisce al ripristino della maturazione delle cellule ematopoietiche e alla produzione dei globuli rossi. La molecola ha mostrato risultati promettenti in uno studio di fase 2. MEDALIST è uno studio di fase 3 ideato per testare l’efficacia di luspatercept nei pazienti con anemia associata a sindrome mielodisplastica (MDS) con sideroblasti ad anello, a basso rischio, trasfusione-dipendenti per fallimento, intolleranza o ineleggibilità a terapia con agenti stimolanti l'eritropoiesi. I risultati dello studio sono stati recentemente pubblicati sul NEJM.
Pazienti e metodi
Lo studio multicentrico di fase 3, in doppio cieco, ha arruolato 229 pazienti, affetti da MDS con sideroblasti ad anello, a rischio molto basso, basso o intermedio secondo il Revised International Prognostic Scoring System (RISS). Tutti necessitavano di almeno due trasfusioni eritrocitarie ogni due mesi ed erano non idonei, intolleranti o non rispondenti agli ESA. I pazienti sono stati randomizzati con rapporto 2:1 a ricevere luspatercept (da 1,0 a 1,75 mg/kg) o placebo per via sottocutanea ogni tre settimane. L'endpoint primario era l'indipendenza trasfusionale per 8 settimane o più nelle prime 24 settimane. L'endpoint secondario era l'indipendenza trasfusionale per almeno 12 settimane, valutata nelle prime 24 e nelle prime 48 settimane di trattamento.
Risultati
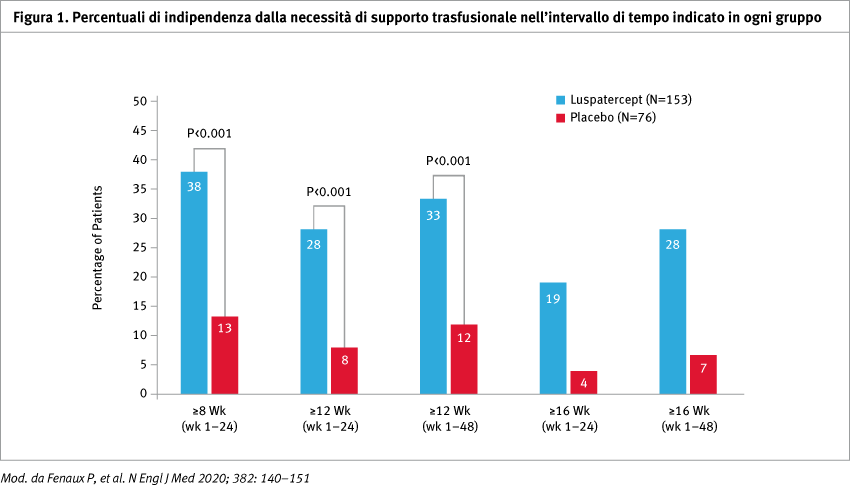
Dei 229 pazienti arruolati, 153 sono stati trattati nel braccio luspatercept e 76 nel braccio placebo; le caratteristiche basali dei due gruppi erano bilanciate. Il trattamento con luspatercept ha determinato un miglioramento nei due endpoints: l'indipendenza trasfusionale per almeno 8 settimane è stata osservata nel 38% dei pazienti nel gruppo sperimentale, rispetto al 13% nel gruppo placebo (p <0,001). Analogamente, una percentuale più alta di pazienti nel gruppo luspatercept rispetto al gruppo placebo ha raggiunto l'endpoint secondario principale, l'indipendenza trasfusionale per almeno 12 settimane (28% contro 8% per le settimane da 1 a 24 e 33% contro 12% per le settimane da 1 a 48; p <0,001 per entrambi) (Figura 1).
Il profilo di sicurezza di luspatercept è risultato coerente con quello riportato per il farmaco nello studio di dose-finding di fase 2. Gli eventi avversi più comuni associati a luspatercept includevano affaticamento, diarrea, astenia, nausea e vertigini. L'incidenza di eventi avversi è diminuita nel tempo.
Conclusioni
Luspatercept è efficace nel ridurre la gravità dell'anemia nei pazienti con MDS con sideroblasti ad anello trasfusione-dipendenti refrattari o intolleranti agli agenti stimolanti l'eritropoiesi, è ben tollerato e si propone come un’alternativa al supporto trasfusionale associato alla terapia ferrochelante in questo setting di pazienti.