Numero speciale di "Impact Factor News” n° 1 - Aprile 2020
Introduzione
La terapia cellulare con linfociti T modificati per esprimere il recettore antigenico chimerico (CAR) anti-CD19 ha dimostrato notevole efficacia clinica nei tumori a cellule B. Tuttavia, vi sono ancora alcune difficoltà nell’applicazione su larga scala di questi trattamenti, rappresentate sia dalla complessità di realizzazione di questi prodotti cellulari, sia dagli effetti tossici sostanziali da loro indotti, in primis la sindrome da rilascio citochinico e la neurotossicità. In questo lavoro gli sperimentatori presentano i dati di efficacia di un prodotto cellulare di cellule natural killer (NK) che sono state modificate per esprimere un CAR anti-CD19 e che hanno il potenziale per superare le due principali tossicità.
Pazienti e metodi
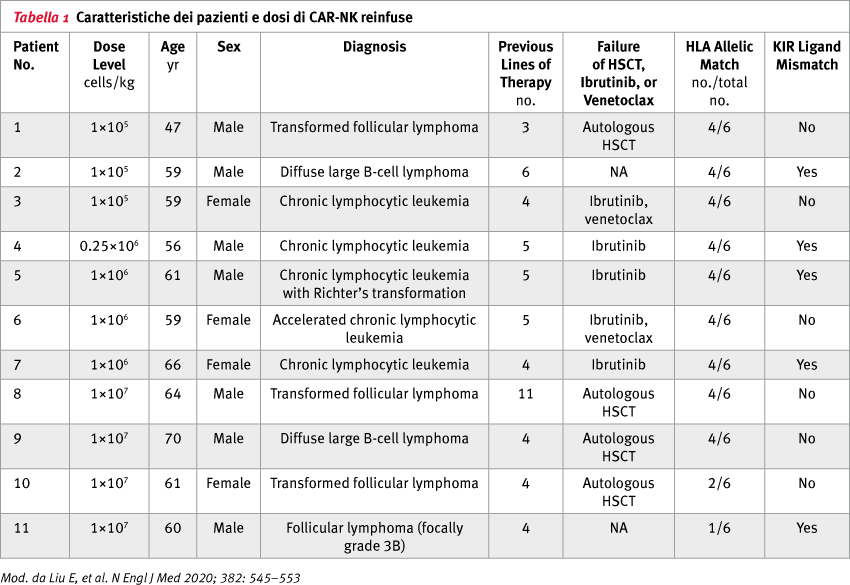
In questo studio di fase 1 -2, gli sperimentatori hanno somministrato CAR-NK anti-CD19 di cellule HLA-mismatched derivate dal sangue cordonale a 11 pazienti con tumori CD19-positivi istotipi: linfoma non Hodgkin B (LNH-B) o leucemia linfatica cronica (BLLC) nel setting della malattia recidivata/refrattaria (Tabella 1). Le cellule NK sono state trasdotte con un vettore retrovirale che esprime geni che codificano CAR anti-CD19, interleuchina-15 e la caspasi inducibile 9, come interruttore di sicurezza.Le cellule sono state espanse ex vivo e somministrate in un'unica infusione in una delle tre seguenti dosi: 1 × 105, 1 × 106 o 1 × 107 cellule CAR-NK/kg di peso corporeo dopo somministrazione di una chemioterapia con effetto linfodepletivo. Studio sponsorizzato dal M.D. Anderson Cancer Center CLL e Linfoma Moonshot e National Institutes of Health; registrato su ClinicalTrials.gov, NCT03056339.
Risultati
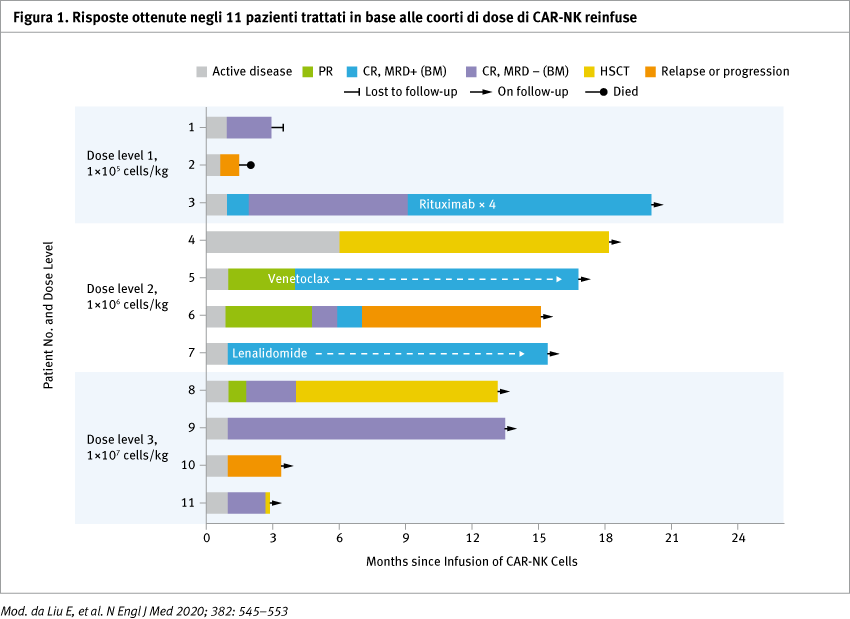
La somministrazione di cellule CAR-NK non è stata associata allo sviluppo di sindrome da rilascio di citochine, neurotossicità o malattia da trapianto verso l'ospite. Inoltre, non è stato osservato alcun aumento dei livelli di citochine infiammatorie, compresa l'interleuchina-6, al di sopra del range di normalità. Non è stata raggiunta la dose massima tollerata. Degli 11 pazienti che sono stati trattati, 8 (73%) hanno avuto una risposta oggettiva; di questi pazienti, 7 (4 con linfoma e 3 con BLLC) hanno ottenuto una remissione completa, e 1 ha ottenuto una regressione della componente trasformata di malattia (regressione del foce di Sindrome di Richter) mantenendo la componente di BLLC in modo persistente. Le risposte sono state rapide e visibili entro 30 giorni dall'infusione a tutti i livelli di dose. Le cellule CAR-NK infuse si sono inoltre espanse in vivo e hanno presentato una persistenza a bassi livelli per almeno 12 mesi (Figura 1).
Conclusioni
Gli Autori concludono che l’utilizzo di questo prodotto cellulare in 11 pazienti con tumori recidivati o refrattari CD19-positivi, ha permesso di far ottenere alla maggioranza di loro una risposta al trattamento con cellule CAR-NK senza lo sviluppo dei noti effetti collaterali e senza lo sviluppo di nuovi importanti effetti tossici.