Numero speciale di "Impact Factor News” n° 1 - Aprile 2021
Introduzione
Nel 2012 Treon et al. hanno dimostrato, con il sequenziamento genico, che il 90% dei pazienti con macroglobulinemia di Waldenström (WM) presentava la mutazione puntiforme L265P di MYD88. Gli effetti biologici di questa mutazione includono l'attivazione della tirosin chinasi di Bruton (BTK) e altri effetti a valle; di conseguenza, l’inibizione di BTK diventava il razionale per un approccio terapeutico a questa malattia.Infatti, nello stesso anno partiva lo studio con ibrutinib in monoterapia in 63 pazienti con WM recidivanti/refrattari. Lo studio otteneva alti tassi di risposta e dati di sopravvivenza superiori a qualsiasi altro trattamento fino a quel momento utilizzato, seppur con follow-up molto breve. Di conseguenza, ibrutinib è stato il primo agente terapeutico approvato formalmente nella WM ed è diventato per molti medici il trattamento di scelta per i pazienti con malattia recidivante/refrattaria. In questo lavoro vengono riportati i risultati a lungo termine di questo studio pilota.
Metodi
Lo studio ha arruolato 63 pazienti sintomatici precedentemente trattati, di cui il 40% era refrattario all’ultimo trattamento con una media di due linee precedenti (range 1–9). La dose di ibrutinib somministrata era pari a 420 mg/die, come da dosaggio della BLLC/SLL (leucemia linfatica cronica/linfoma a piccoli linfociti). Una riduzione della dose era consentita in caso di tossicità.
Risultati
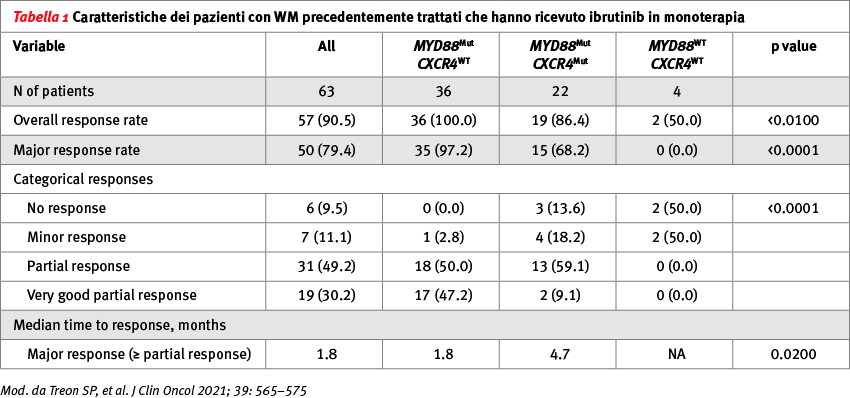
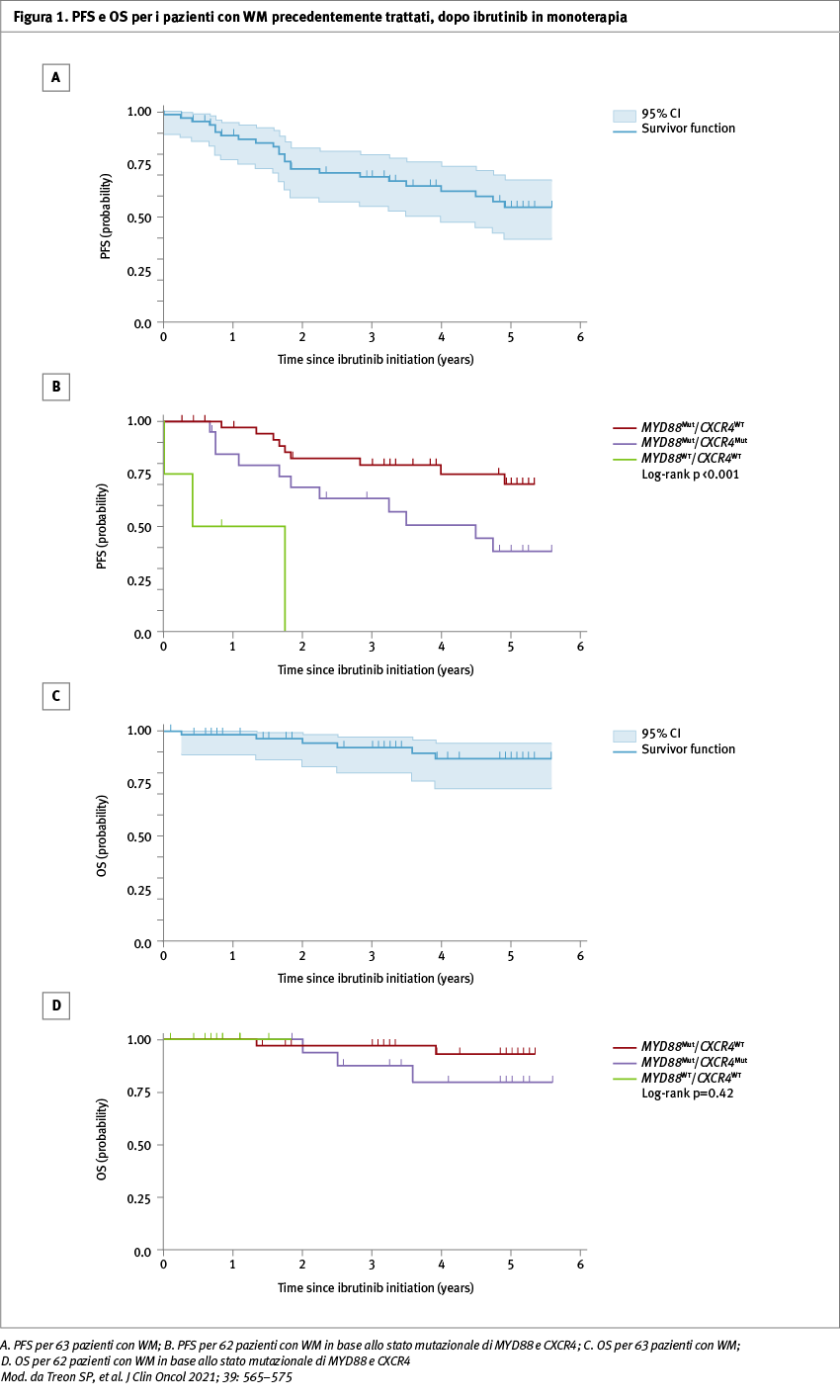
I tassi di risposta globale e maggiore sono stati rispettivamente del 90,5 e del 79,4%. Si è inoltre osservato che il tasso di risposta parziale molto buona (VGPR) migliora nel tempo anche se nessun paziente ha raggiunto una risposta completa (CR). Con una mediana di 59 mesi di follow-up, il 54% dei pazienti rimane libero da progressione a cinque anni, e questo, anche in assenza di dati formali randomizzati, appare significativamente superiore alle terapie convenzionali in caso di ricaduta, compreso il trapianto autologo di cellule staminali. La progression-free survival (PFS) è influenzata dal numero di precedenti linee di terapia, dall’infiltrato di malattia del midollo osseo, dal punteggio dell’IPSSWM (International Prognostic Scoring System WM), ma non dai livelli di IgM o dalla refrattarietà alla terapia precedente.Le risposte sono state influenzate dallo stato mutazionale di MYD88 e CXCR4.Pazienti con mutazione di MYD88 ed espressione normale di CXCR4 (MYD88MutCXCR4WT) hanno mostrato una risposta maggiore nel 97,2 vs 68,2% (p <0,0001), una risposta parziale molto buona nel 47,2 vs 9,1% (p <0,01), e un tempo all’ottenimento della risposta maggiore più breve di 1,8 vs 4,7 mesi (p=0,02) rispetto a pazienti con mutazione sia di MYD88 sia di CXCR4 (MYD88MutCXCR4Mut).Al contrario, quattro pazienti che avevano la malattia MYD88WT non hanno mostrato risposte maggiori. Il tempo mediano della PFS a cinque anni per tutti i pazienti non è stato raggiunto. A cinque anni la PFS è stata del 70% nei pazienti MYD88MutCXCR4WT e del 38% per quelli con MYD88MutCXCR4Mut (p=0,02) (Tabella 1). Nei pazienti con MYD88WT, la PFS mediana era di 0,4 anni (p <0,01). L’overall survival (OS) a cinque anni per tutti i pazienti è stata dell'87%, senza differenze statisticamente significative tra i due sottogruppi (MYD88MutCXCR4WT e MYD88MutCXCR4Mut) (Figura 1). Gli eventi avversi di grado severo, correlati al farmaco, hanno incluso: neutropenia (15,9%), trombocitopenia (11,1%) e polmonite (3,2%). Otto pazienti (12,7%) hanno presentato disturbi del ritmo atriale, la quasi totalità di questi (7/8) ha comunque continuato la terapia con il supporto farmacologico cardiologico specifico senza sequele.
Conclusioni
Gli autori concludono che ibrutinib si riconferma essere una terapia altamente attiva e tollerabile nei pazienti con WM pluritrattati, con risposte che si mantengono a lungo termine nella maggior parte dei pazienti. Rispetto ad altre terapie disponibili, l'efficacia e la sicurezza a lungo termine di ibrutinib rendono l’inibitore di BTK un'opzione preferibile per WM precedentemente trattata in assenza di studi prospettici randomizzati.


