Numero speciale di "Impact Factor News” n° 1 - Aprile 2022
Introduzione
La maggior parte dei pazienti con diagnosi di linfoma mantellare (MCL) ha più di 65 anni. L'età, congiuntamente con il performance status e il numero di comorbidità, è predittiva degli esiti clinici in questa popolazione di pazienti. Il trattamento standard per i pazienti anziani con MCL è basato sulla chemioimmunoterapia, tuttavia questa strategia determina un alto grado di tossicità. Gli inibitori della tirosin-chinasi di Bruton, come ibrutinib, hanno mostrato risultati promettenti in studi clinici precedenti nel MCL. Jain e colleghi hanno valutato la sicurezza e l'efficacia della combinazione chemo-free ibrutinib + rituximab (IR) nei pazienti anziani con MCL non precedentemente trattato, con risultati interessanti.
Metodi
Lo studio, monocentrico, di fase II non randomizzato, ha arruolato 50 pazienti con MCL di nuova diagnosi (NCT01880567). I pazienti con Ki-67% ≥50% e morfologia blastoide sono stati esclusi dal trial. Ibrutinib è stato somministrato in combinazione con rituximab nei primi due anni di terapia e, quindi, proseguito continuativamente in monoterapia. L'obiettivo principale era valutare il tasso di risposta globale e la sicurezza della combinazione IR.
Risultati
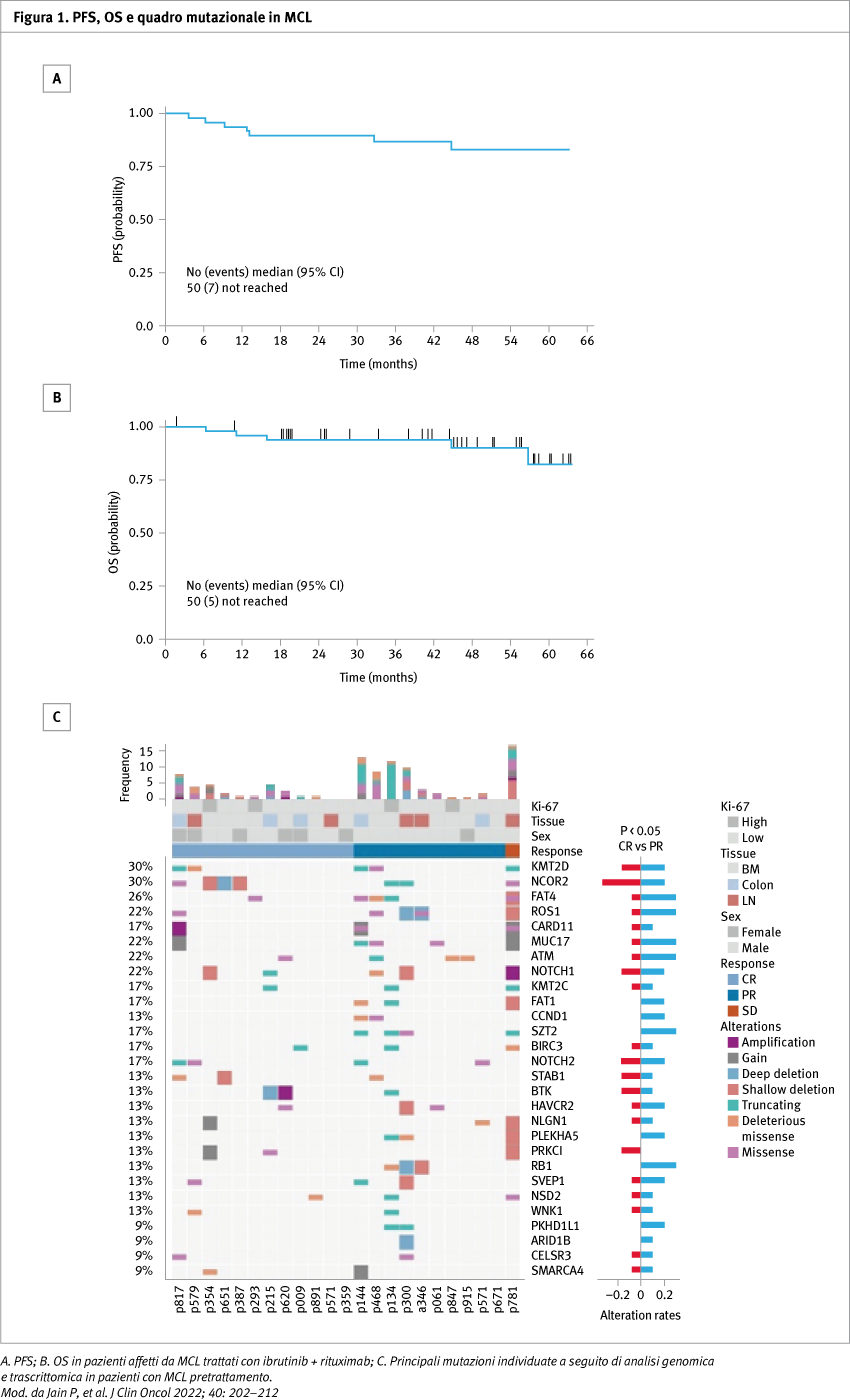
Complessivamente, sono stati inclusi 50 pazienti con età media di 71 anni (range 65–84), il 77% dei quali era di sesso maschile, il 98% aveva un punteggio di Eastern Cooperative Oncology Group performance status (ECOG PS) pari a 0-1. Il 16% dei pazienti aveva un MCL International Prognostic Index (IPI) ad alto rischio. Il Ki-67 era basso (<30%) nel 76% dei pazienti e moderatamente alto (≥30%–50%) nel 24%. Il 94% dei pazienti aveva coinvolgimento midollare e il 48% aveva la malattia in stadio IV. Il follow-up mediano è stato di 45 mesi, durante i quali il 56% dei pazienti ha interrotto il trattamento per una serie di motivi, tra cui tossicità (21 pazienti) e progressione della malattia (4 pazienti). Tra i pazienti valutabili, la risposta obiettiva è stata osservata nel 96% dei casi, con una risposta completa nel 71% dei pazienti. La sopravvivenza mediana libera da progressione e quella globale non sono state raggiunte; i tassi di sopravvivenza libera da progressione e globale a tre anni corrispondevano, rispettivamente, all'87% e al 94% (Figura 1). Non sono stati registrati decessi durante il periodo di studio. Gli eventi avversi più comuni di grado 3 o 4 sono stati fibrillazione atriale (FA, 22%), fatigue (18%), diarrea (14%) e mialgia (14%). Le tossicità ematologiche di grado 3 o 4 consistevano in neutropenia nell'8% dei pazienti, anemia nel 4% e trombocitopenia nel 4%. Quattro pazienti hanno manifestato sanguinamento di grado 3 o 4 in corso di ibrutinib. Complessivamente, 17 pazienti (34%) hanno sviluppato FA, di cui nove non avevano storia precedente di malattia. La FA ha comportato l'interruzione di ibrutinib in 10 partecipanti. Non sono stati osservati decessi correlati al trattamento. L’analisi genomica e trascrittomica integrata sulle biopsie eseguite pretrattamento ha dimostrato il significato delle aberrazioni del pathway del B-cell receptor come predittore della risposta ad ibrutinib, con pattern differente di espressione di CCND1, BIRC3, BANK1, SETBP1, AXIN2 e IL2RA in chi non otteneva la remissione completa (Figura 1).
Conclusioni
La combinazione IR ha dimostrato tassi di risposta elevati e sopravvivenza duratura nei pazienti anziani con MCL. La valutazione di base del rischio cardiovascolare è altamente raccomandata. Come atteso, la tossicità non ematologica prevalente era rappresentata dalla fibrillazione atriale. Gli autori concludono che uno studio randomizzato potrebbe definire il ruolo di questa interessante combinazione nell’anziano affetto da MCL.


