Numero speciale di "Impact Factor News” n° 1 - Aprile 2022
Introduzione
L’outcome clinico dei linfomi non-Hodgkin aggressivi a cellule B che non rispondono o progrediscono entro 12 mesi dalla terapia di prima linea è spesso insoddisfacente. Tisagenlecleucel (tisa-cel) è una terapia a cellule T con recettore dell’antigene chimerico (CAR-T) anti-CD19, il cui uso è attualmente approvato nel linfoma diffuso a grandi cellule B (DLBCL) dopo almeno due linee di trattamento.
Metodi
Lo studio internazionale di fase III BELINDA ha coinvolto pazienti con linfoma aggressivo refrattario o in progressione entro 12 mesi dalla terapia di prima linea. I pazienti sono stati assegnati in modo casuale a ricevere tisa-cel con terapia ponte opzionale (gruppo tisa-cel) o chemioterapia di salvataggio e trapianto autologo di cellule staminali ematopoietiche (ASCT) (gruppo SoC). L'endpoint primario era la sopravvivenza libera da eventi (EFS), definita come il tempo dalla randomizzazione alla malattia stabile o progressiva alla settimana 12 (o oltre) o al decesso. In caso di evento di progressione/recidiva dopo la settimana 12, era possibile il crossover per ricevere tisa-cel. Tra gli endpoints secondari si segnalano il tasso di risposta e la safety.
Risultati
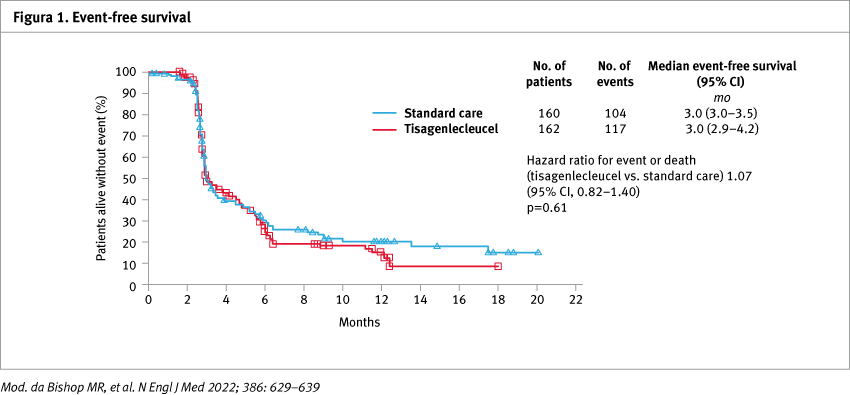
Nel trial sono stati randomizzati 322 pazienti con rapporto 1:1. Al baseline, la percentuale di pazienti con linfomi ad alto grado era più alta nel gruppo tisa-cel rispetto al gruppo in SoC (24,1 vs 16,9%), così come la percentuale con un punteggio International Prognostic Index (IPI) ≥2 (65,4 vs 57,5%). All’analisi dei dati, il follow-up mediano è stato di 10 mesi. Il 96,9% dei pazienti nel gruppo standard di cura ha ricevuto almeno due cicli di chemioterapia e il 53,8% ha ricevuto almeno due regimi. Il 32,5% dei pazienti nel gruppo SoC ha ricevuto ASCT, di cui il 31% ha ricevuto due diversi regimi chemioterapici prima dell'ASCT. Il tempo mediano dalla randomizzazione al trapianto è stato di 3,0 mesi (range 2,0–5,2 mesi). Complessivamente, il 15,6% dei pazienti è diventato non idoneo al trapianto durante il periodo di trattamento per ragioni diverse dalla risposta inadeguata. Al cutoff dei dati, il 50,6% dei pazienti nel gruppo SoC aveva effettuato il crossover e aveva ricevuto tisa-cel. Il 25,9% dei pazienti nel gruppo tisa-cel ha avuto una progressione del linfoma alla sesta settimana rispetto al 13,8% di quelli nel gruppo SoC. Nel trial, l’endpoint primario non è stato soddisfatto: la EFS mediana era identica nei due gruppi ed era pari a 3,0 mesi (hazard ratio, HR per evento o morte nel gruppo tisa-cel 1,07; 95% confidence interval, CI: 0,82–1,40; p=0,61) (Figura 1). EFS e sopravvivenza globale (OS) erano più brevi tra i pazienti con linfoma a cellule B di alto grado in entrambi i gruppi rispetto ai pazienti con linfoma primario a cellule B mediastinico o DLBCL. Per quanto riguarda la risposta al trattamento, l’overall response rate (ORR) era del 46,3% nei pazienti del gruppo tisa-cel e del 42,5% nel gruppo con SoC (Tabella 1). Dieci pazienti nel gruppo tisa-cel e 13 nel gruppo SoC sono morti a causa di eventi avversi.
Conclusioni
Nel trial BELINDA, tisa-cel non si è dimostrato superiore alla terapia di salvataggio standard, in contrasto con i risultati dello studio ZUMA -7. I ricercatori hanno identificato alcuni fattori che potrebbero aver potenzialmente contribuito ai risultati insoddisfacenti del trial. Tra questi, l’uso non uniforme della terapia ponte che ha portato a un numero maggiore di pazienti con malattia progressiva all'infusione (sesta settimana, progressione 25,9 vs 13,8%), che è stata associata ad un esito peggiore. In particolare, i pazienti trattati in centri non statunitensi tendevano a ricevere più cicli di chemioterapia transitoria. In aggiunta, il tempo all’infusione: i pazienti hanno atteso una mediana di 52 giorni per la loro infusione di cellule CAR-T dopo la leucaferesi, tempo relativamente lungo data la natura aggressiva della malattia. Inoltre, i pazienti nel braccio standard di cura potevano ricevere fino a due diversi regimi prima che la strategia fosse considerata un fallimento. I ricercatori hanno anche notato alcune differenze potenzialmente significative tra i bracci di trattamento in specifici gruppi di pazienti in termini di biologia della malattia e fattori prognostici. Ulteriori studi potranno chiarire il ruolo delle CAR-T in questo setting di pazienti.