Numero speciale di "Impact Factor News” n° 1 - Aprile 2023
Introduzione
I regimi di condizionamento mieloablativo basati sull'irradiazione corporea totale (TBI) sono ampiamente utilizzati nella leucemia linfoblastica acuta (ALL). Il ruolo dei regimi mieloablativi a base di busulfano (Bu) in questo contesto clinico rimane oggetto di discussione. In questo studio randomizzato, condotto da ricercatori cinesi in pazienti affetti da ALL-B a rischio citogenetico standard e candidati ad allotrapianto (allo-HSCT) da donatore HLA identico in prima remissione completa (CR1), sono state confrontate l'efficacia e la sicurezza di regimi di condizionamento basati sull’utilizzo di Bu e ciclofosfamide (BuCy) in confronto al condizionamento basato sulla TBI più ciclofosfamide (TBI-Cy).
Metodi
Lo studio di fase III, randomizzato, in aperto, è stato condotto in 13 ospedali in Cina. I pazienti eleggibili (età 14–65 anni) presentavano ALL a rischio standard in CR1. I pazienti sono stati randomizzati con rapporto 1:1 a ricevere un condizionamento con BuCy (0,8 mg/kg 4 volte al giorno nei giorni da –7 a –4 e ciclofosfamide 60 mg/kg/die nei giorni da –3 a –2) o TBI-Cy (4,5 Gy TBI nei giorni da –5 a –4 e ciclofosfamide 60 mg/kg/die nei giorni da –3 a –2). L'endpoint primario è stata la sopravvivenza globale (OS) a due anni.
Risultati
Tra gennaio 2016 e febbraio 2020, lo studio ha incluso 550 pazienti, di cui 275 sono stati randomizzati a ricevere BuCy (valutabili 273, età mediana 26 anni, range 14–59) e 275 a ricevere TBI-Cy (valutabili 272, età mediana 27 anni, range 14–61). L’OS a due anni nel gruppo BuCy (76,6%; confidence interval CI 95%: 71,7–81,8) non è stata inferiore a quella del gruppo TBI-Cy (79,4%; CI 95%: 74,7–84,4; p=0,457; differenza 2,9%; CI 95%: -4,1–9,8; p=0,022). Analogamente, il tasso di recidive a due anni è stato del 20,2% (CI 95%: 15,6–25,1) e del 18,4% (14,0– 23,2; p=0,616) e la mortalità senza recidiva è stata dell'11,0% (CI 95%: 7,6–15,0) e dell'11,0% (7,7–15,1; p <0,988), rispettivamente, nel gruppo BuCy e nel gruppo TBI-Cy (Figura 1).
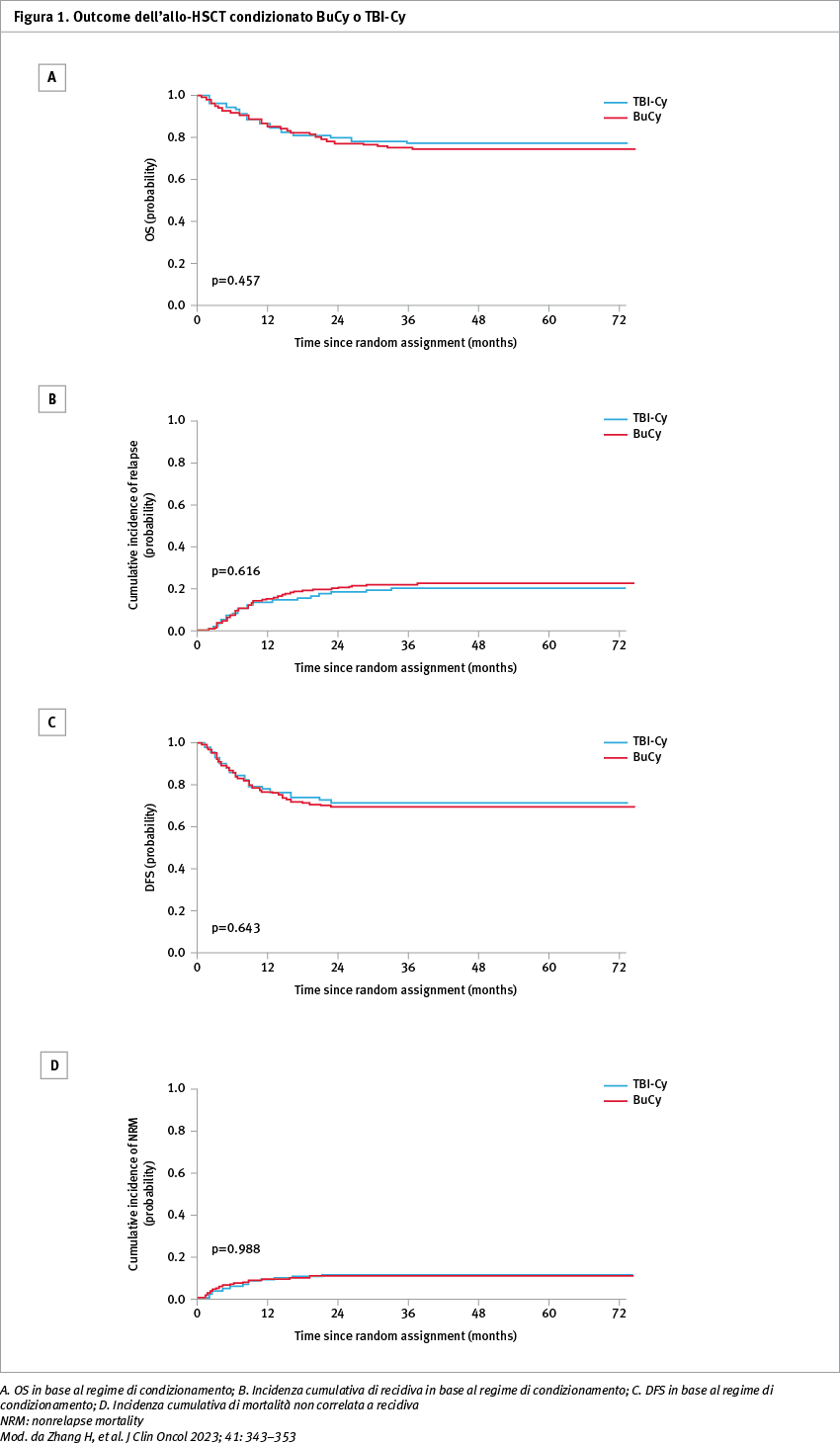
Non sono state riscontrate differenze nella tossicità correlata al regime, nella malattia del trapianto contro l'ospite o negli eventi a lungo termine tra i due gruppi.
Conclusioni
Gli autori concludono che il regime BuCy ha un’efficacia e una sicurezza non inferiori a TBI-Cy (4,5 Gy x 2) per i pazienti adulti con ALL-B a rischio standard in CR1 sottoposti ad allo-HSCT da donatore HLA identico. Questo studio identifica il regime BuCy come un possibile condizionamento alternativo in questo setting di pazienti.


