Numero speciale di "Impact Factor News” n° 1 - Aprile 2023
Introduzione
L’inibitore di FLT3 gilteritinib è altamente attivo nella leucemia mieloide acuta (AML) avanzata con mutazione di FLT3 (FLT3-mut), ma non è curativo; infatti, nonostante il suo ruolo di terapia standard nella AML recidivata/refrattaria FLT3-mutata, raramente induce risposte prolungate. In fase preclinica, l'inibitore di BCL-2 venetoclax ha dimostrato un’azione sinergica con gilteritinib in modelli di AML FLT3-mut. Sul Journal of Clinical Oncology, Daver ha presentato i risultati dello studio di fase Ib che, in base alla presupposta possibilità di ottenere una riduzione precoce e profonda del clone FLT3-mut mediante la combinazione dei due farmaci orali, ne ha testato con successo la tollerabilità e l’efficacia.
Metodi
Lo studio di fase Ib, in aperto, dose-escalation/dose-expansion, ha arruolato pazienti con AML recidivata/refrattaria FLT3 wild-type e FLT3-mut (dose-escalation) o FLT3-mut (dose-expansion). I pazienti hanno ricevuto 400 mg di venetoclax per os una volta al giorno e gilteritinib 80 mg o 120 mg per os una volta al giorno. Gli obiettivi primari sono stati la sicurezza, l'identificazione della dose raccomandata per la fase II e il tasso di risposte complete composite modificato (mCRc) (risposta completa [CR] + CR con recupero incompleto della conta ematica + CR con recupero piastrinico incompleto + risposta morfologica) utilizzando i criteri di risposta dello studio di fase III ADMIRAL.
Risultati
Lo studio ha arruolato 61 pazienti (FLT3-mut n=56); il 64% (36/56) dei pazienti con FLT3-mut aveva ricevuto precedente terapia con inibitori di FLT3. Al termine della fase di dose-escalation, la dose raccomandata è stata di 400 mg di venetoclax e 120 mg di gilteritinib in mono-somministrazione giornaliera. Per quanto riguarda la tollerabilità, la principale tossicità è stata la mielosoppressione, gestibile con la modifica dei dosaggi. Gli eventi avversi di grado 3/4 più comuni sono stati infatti le citopenie (n=49; 80%). Si è resa necessaria l'interruzione temporanea della dose di venetoclax e gilteritinib nel 51 e nel 48% dei pazienti, rispettivamente. La mortalità precoce con venetoclax + gilteritinib è stata simile a quella osservata con gilteritinib in monoterapia. Il follow-up mediano è stato di 17,5 mesi. La terapia di combinazione si è dimostrata efficace, con un tasso di risposte elevato (mCRc nei pazienti con FLT3-mut: 75%; CR: 18%; CR con recupero incompleto della conta ematica: 4%; CR con recupero piastrinico incompleto: 18%; remissione morfologica: 36%). La percentuale di risposte è stata simile nei pazienti precedentemente esposti o non esposti a inibitori di FLT3 (67 e 80%, rispettivamente). Il tempo mediano alla risposta è stato di 0,9 mesi e la durata mediana della remissione è stata di 4,9 mesi (confidence interval, CI 95%: 3,4–6,6) (Figura 1).
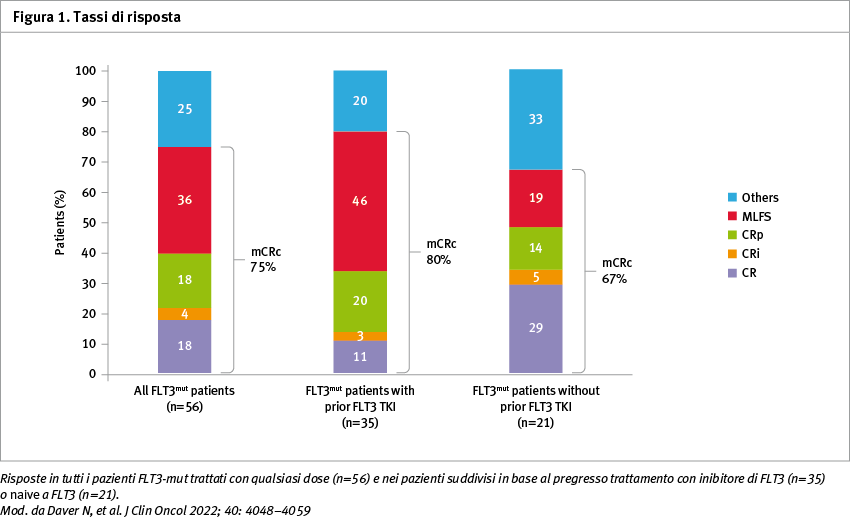
La risposta molecolare (FLT3 <10-2) è stata raggiunta nel 60% dei pazienti valutabili che avevano ottenuto una mCRc (15/25). La sopravvivenza globale per i pazienti con FLT3-mut è stata di 10,0 mesi (Figura 2).
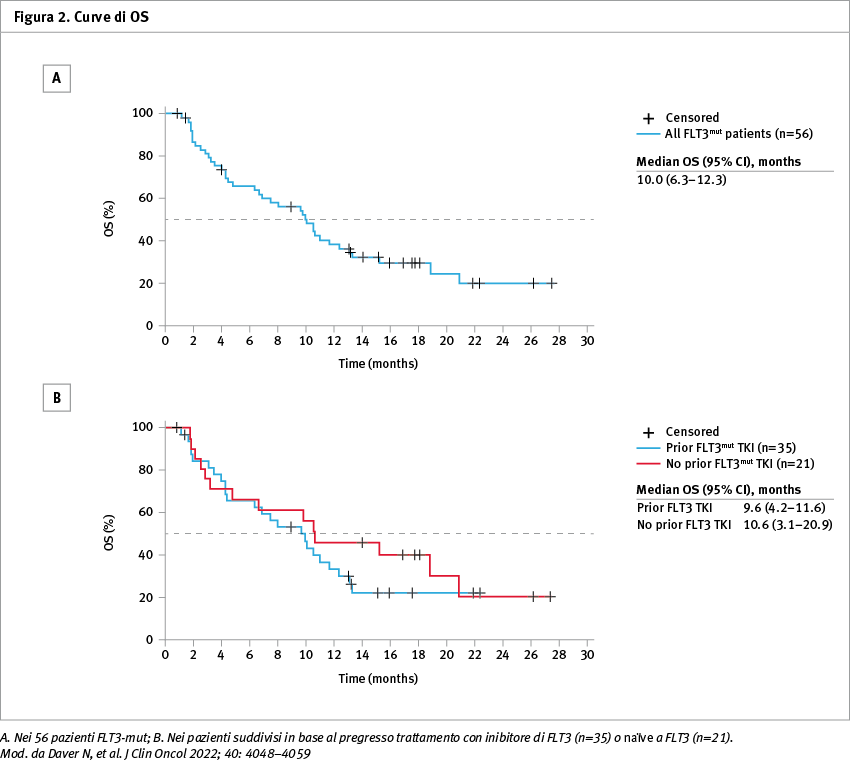
Conclusioni
Gli autori concludono che, nei pazienti con AML ad alto rischio per FLT3-mut, la combinazione ad assunzione orale di venetoclax + gilteritinib è altamente attiva, tollerabile e potenzialmente migliora la percentuale e la profondità della risposta rispetto agli standard terapeutici disponibili.


