Numero speciale di "Impact Factor News" n° 3 - Aprile 2026
Introduzione
I pazienti con mieloma extramidollare (plasmacitoma non a partenza scheletrica) hanno un elevato rischio di progressione/recidiva di malattia che ne condiziona negativamente la prognosi. Nella fase 1, lo studio RedirecTT-1 ha mostrato un’efficacia promettente con il doppio targeting antigenico derivato dalla combinazione di talquetamab (anti–GPRC5D) e teclistamab (anti–BCMA) in pazienti con mieloma multiplo (MM) recidivato o refrattario (R/R) già esposti alle tre classi principali di farmaci, inclusi i pazienti con mieloma extramidollare.
Metodi
Lo studio di fase 2 RedirecTT-1 ha valutato la combinazione talquetamab + teclistamab esclusivamente in pazienti con mieloma extramidollare farmaco-resistente. L’endpoint primario dello studio era il tasso di risposta globale (ORR), valutato mediante imaging funzionale. Gli endpoints secondari includevano la durata della risposta, la sopravvivenza libera da progressione (PFS), la sopravvivenza globale (OS) e la valutazione della sicurezza.
Risultati
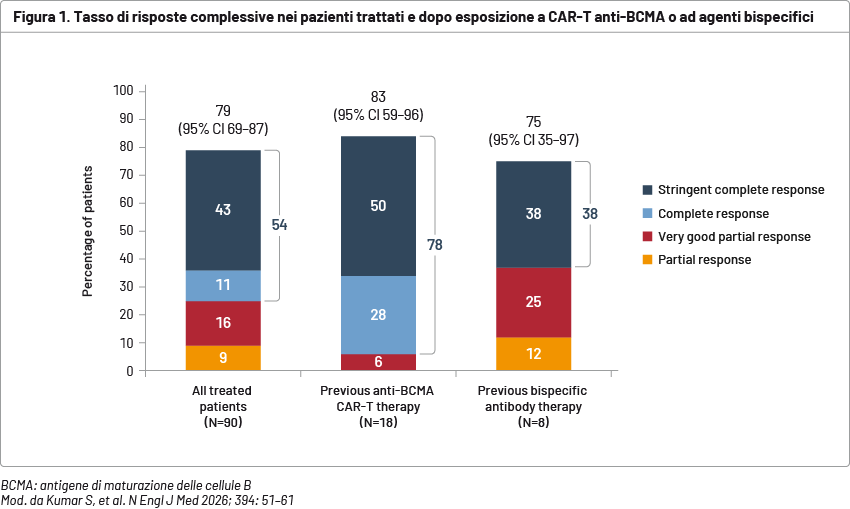
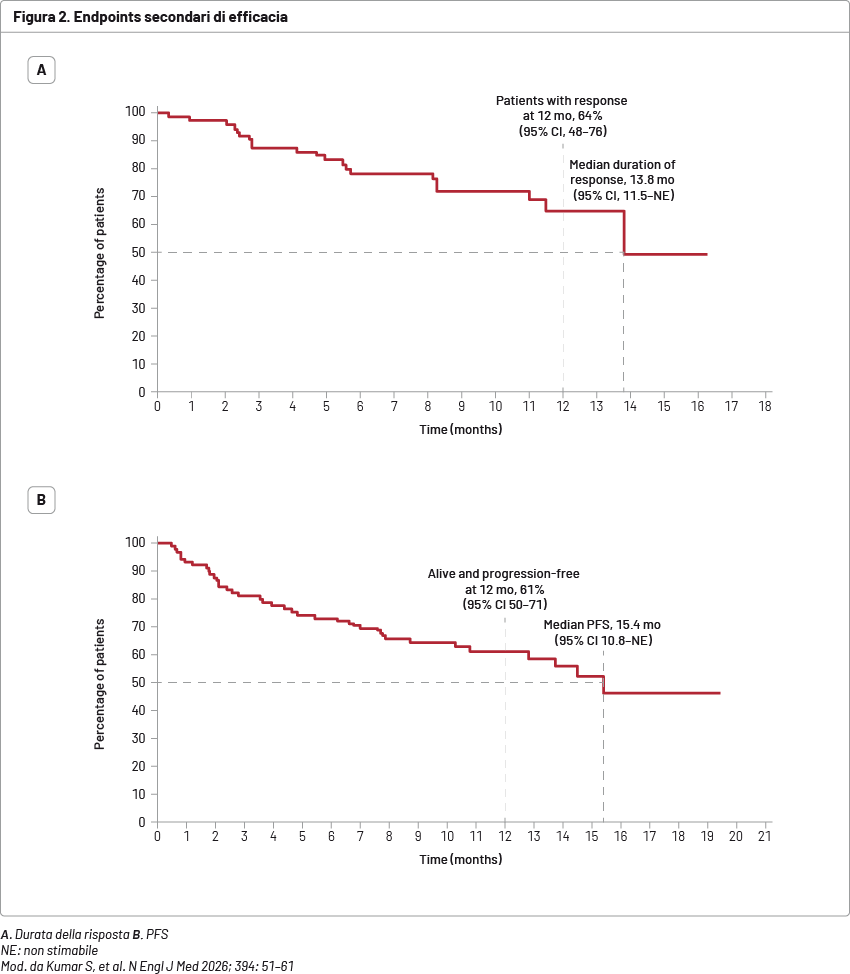
In totale, lo studio ha arruolato 90 pazienti. Con un follow-up mediano di 12,6 mesi, sono stati riscontrati i seguenti risultati: risposta globale 79% (Figura 1); durata della risposta ≥12 mesi (nei responders) 64% (Figura 2A); PFS a 12 mesi 61% (Figura 2B); OS a 12 mesi 74%.
Per quanto riguarda la sicurezza, gli eventi avversi (EA) comuni di qualsiasi grado includevano la sintomatologia orale (87%), la sindrome da rilascio di citochine (78%) e la tossicità cutanea non rash (69%). Gli EA di grado 3 o 4 erano per lo più ematologici e si erano verificati nel 76% dei pazienti. Il 31% ha presentato infezioni di grado 3 o 4. Il tasso di sospensione di uno o entrambi i farmaci per EA è stato del 6%. Per quanto riguarda i 10 decessi verificatisi durante il follow-up, 5 erano dovuti a infezioni e 5 erano considerati correlati al trattamento.
Conclusioni
Il doppio targeting terapeutico con la combinazione di teclistamab e talquetamab ha determinato un’attività significativa in un setting di pazienti ad altissimo rischio biologico, con un profilo di tossicità rilevante ma coerente con i singoli agenti. (Finanziato da Johnson & Johnson; numero ClinicalTrials.gov, NCT04586426).


