Numero speciale di "Impact Factor News” n° 3 - Ottobre 2014
Introduzione
Le sindromi mielodisplastiche (MDS) sono un gruppo eterogeneo di patologie per manifestazioni cliniche, alterazioni citogenetiche e molecolari, prognosi. Le mutazioni puntiformi somatiche ricorrenti sono riconosciute come evento patogenetico nelle MDS e si possono associare a manifestazioni fenotipiche. Tali mutazioni sono prognosticamente importanti anche in termini di risposta agli agenti ipometilanti.
Su Journal of Clinical Oncology sono stati presentati i risultati di uno studio volto a valutare l’impatto prognostico della presenza di mutazioni somatiche nei pazienti candidati a trapianto.
L’identificazione di elementi di supporto nel calcolare il rapporto rischio-beneficio e il timing del trapianto è un’esigenza particolarmente sentita nei pazienti affetti da MDS, caratterizzati da età avanzata con conseguente carico di comorbidità.
Pazienti e metodi
I campioni basali di 87 pazienti affetti da MDS e sottoposti a trapianto allogenico sono stati esaminati con sequenziamento massivo parallelo per 40 mutazioni codificanti note come mutazioni ricorrenti nelle MDS.
Risultati
Gli Autori hanno riscontrato la presenza di mutazioni nel 92% dei pazienti con la seguente frequenza: ASXL1 (29%), TP53 21%, DNMT3A (18%) e RUNX1 16%.
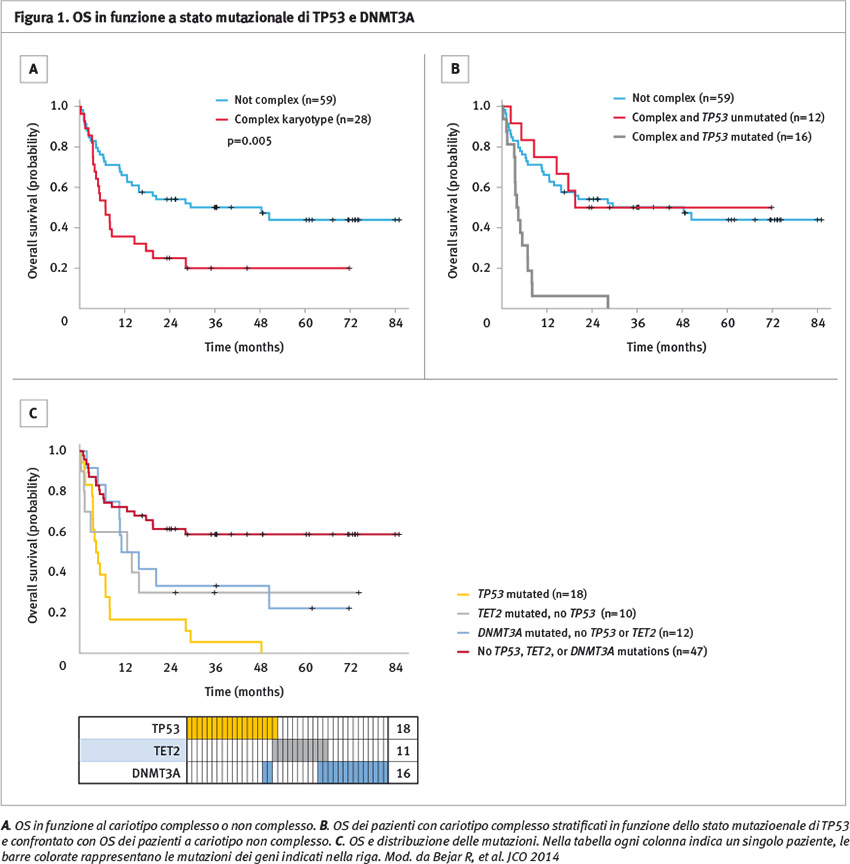
In analisi univariata solo TP53 correlava con una minor OS (HR 3,74 p <0,001) e con una minor PFS (HR 3,97; p <0,001). Dopo correzione per le variabili cliniche associate con questi endpoint le tre mutazioni TP53 (HR 2,3; p=0,27), TET2 (HR 2,4; p=0,033) e DNMT3A (HR 2,08 p=0,049) erano ognuna indipendentemente associata con una minore sopravvivenza dopo trapianto.
Il 46% dei pazienti della popolazione in studio presentava una mutazione di TP53, TET2 o DNMT3A corrispondenti al 64% dei decessi registrati.
La sopravvivenza a tre anni per i pazienti non portatori di mutazioni era del 59% rispetto a una sopravvivenza del 19% in presenza di almeno una mutazione (Figura 1).
Conclusioni
La presenza di mutazioni di TP53, TET2 e DNMT3A identifica un sottogruppo di pazienti con limitata sopravvivenza globale dopo trapianto.
Ad oggi la ricerca di mutazioni genetiche non rientra nella valutazione di routine dei pazienti candidati a trapianto. Gli Autori, pur evidenziando la necessità di ulteriori conferme al loro studio, sottolineano che in presenza di mutazioni prognosticamente sfavorevoli potrebbero essere considerati approcci terapeutici alternativi.