Numero speciale di "Impact Factor News” n° 4 - Ottobre 2019
Background
Il mieloma multiplo (MM) rimane una malattia incurabile nonostante i nuovi trattamenti disponibili abbiano prolungato la sopravvivenza dei pazienti. Anche in questa patologia è in studio l’efficacia delle CAR T-cell. Raje e colleghi hanno presentato sul NEJM i risultati dello studio di fase 1b, CRB-401 disegnato per testare le CAR T-cell bb2121 nei pazienti recidivati refrattari. Le bb2121 sono dirette contro l’antigene di superficie BCMA, espresso dalle plasmacellule sia normali sia tumorali, e in base agli studi preclinici possono avere un ruolo nel trattamento del MM.
Metodi
Lo studio di fase 1 ha arruolato pazienti con MM recidivato o refrattario a ricevere una singola infusione di bb2121 alla dose di 50×106, 150×106, 450×106, o 800×106 cellule CAR-positive (CAR+) T nella fase di dose escalation e 150×106–450×106 cellule CAR+ T nella fase di espansione. Tutti i pazienti erano stati trattati in precedenza con almeno tre linee di trattamento (mediana 7 range 3–23) ed erano stati trattati almeno con un inibitore del proteasoma e con un agente immunomodulatore (IMID) (il 79% dei pazienti era refrattario sia a un inibitore del proteasoma sia a un IMID). L’endpoint primario dello studio era la valutazione della sicurezza del trattamento.
Risultati
Sono stati pubblicati i risultati ottenuti nei primi 33 pazienti infusi con bb2121 con un tempo di osservazione minimo di 6,2 mesi dall’infusione (6,2–22,8).
Gli eventi avversi di grado superiore o uguale a 3 erano prevalentemente di tipo ematologico con una percentuale di neutropenia del 58%, di anemia del 45% e di piastrinopenia del 45%.
L’incidenza della sindrome da rilascio di citochine (CRS) era del 76% ed è stata di grado 1-2 in 23 pazienti (70%) e di grado 3 in soli 2 pazienti (6%). Non ci sono stati casi di CRS di grado 4. L’incidenza di CRS era maggiore nei pazienti che avevano ricevuto più di 150x106 cellule.
Quattordici pazienti (42%) hanno manifestato tossicità neurologica, si è trattato perlopiù di eventi di grado G1-2 (13 pazienti, 39%), in 1 paziente (4%) si è verificata una tossicità neurologica G4 che si è risolta.
Per quanto riguarda l’efficacia, il tasso di risposta complessiva è stato dell’85% compresi 15 pazienti (45%) che hanno ottenuto la remissione completa. Sei dei 15 pazienti in remissione completa sono recidivati.
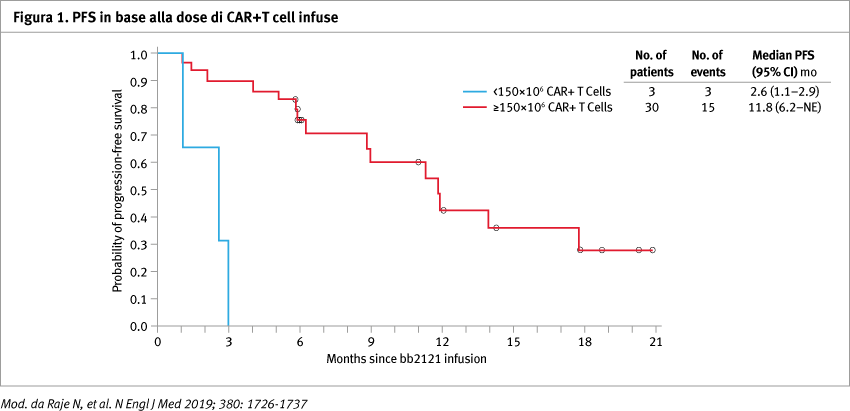
La PFS mediana era di 11,8 mesi (95% IC, 6,2–17,8) (Figura 1). Tutti i 16 pazienti che hanno ottenuto una risposta (RP o superiore nei quali è stata valutata la malattia minima residua (MRD), erano MRD negativi (≤104 cellule nucleate).
L’espansione delle CAR T-cell si associava alla risposta e le cellule CAR T persistevano fino a un anno dall’infusione.
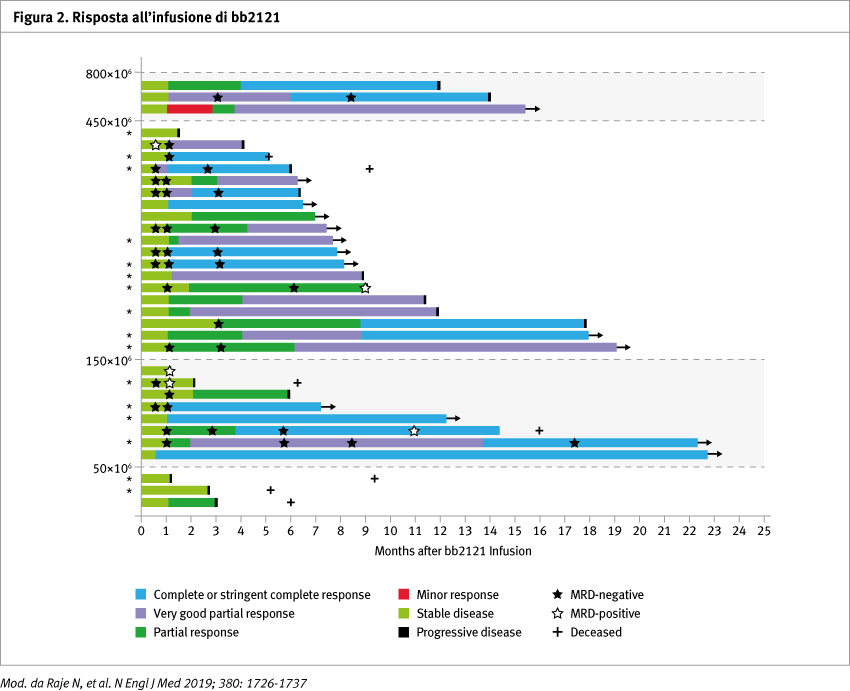
Nella Figura 2 è riportata la miglior risposta al trattamento in base alla dose di cellule infuse (da 50 a 800×106). Tutte le risposte erano confermate e valutate secondo i criteri IMWG. L’asterisco indica i pazienti con elevato carico tumorale (plasmacellule midollari ≥50%).
Conclusioni
Gli Autori riportano gli interessanti risultati preliminari delle CAR T-cell nel mieloma. Lo studio documenta l’attività di bb2121, quando infuse a dosaggio superiore a 150×106 CAR T-cell, in pazienti pesantemente pretrattati, con un profilo di tossicità gestibile.