Numero speciale di "Impact Factor News” n° 4 - Ottobre 2019
Background
Dal momento che la lenalidomide è sempre più utilizzata come terapia di prima linea del mieloma multiplo (MM), i pazienti refrattari a questo trattamento rappresentano un unmet need nella gestione del MM. La combinazione di pomalidomide, bortezomib e desametasone ha mostrato risultati promettenti nello studio di fase 1/2 nei pazienti con MM recidivato refrattario. Lo studio OPTIMISMM è stato disegnato per testare l’efficacia e la sicurezza della tripletta nei pazienti recidivati refrattari precedentemente esposti alla lenalidomide.
Metodi
Lo studio randomizzato, open-label, internazionale di fase 3 ha arruolato pazienti di età ≥18 anni, affetti da MM con malattia misurabile che avessero un ECOG performance status compreso tra 0–2 e che avessero ricevuto da 1 a 3 linee di terapia, compreso un trattamento a base di lenalidomide assunto per almeno 2 cicli consecutivi. I pazienti venivano randomizzati con rapporto 1:1 a ricevere una terapia con bortezomib e desametasone con o senza pomalidomide. I pazienti venivano stratificati in base all’età, il numero di linee di terapia precedenti, la concentrazione di beta-2 microglobulina allo screening.
Bortezomib (1,3 mg/m2) veniva somministrato (ev e successivamente sc dopo emendamento dello studio) nei giorni 1, 4, 8, e 11 per i primi 8 cicli e successivamente nei giorni 1 e 8. Il desametasone al dosaggio di 20 mg (10 mg se età >75 anni) era assunto il giorno di somministrazione di bortezomib e il giorno successivo. I pazienti randomizzati nel gruppo sperimentale assumevano 4 mg di pomalidomide per 15 giorni consecutivi ogni 21 giorni. L’endpoint primario dello studio era la progression-free survival (PFS) in base all’intention-to-treat population, valutata da un comitato indipendente di revisori. La sicurezza è stata valutata in tutti i pazienti che hanno ricevuto almeno una dose dei farmaci in studio.
Risultati
Tra gennaio 2013 e maggio 2017 lo studio ha arruolato 559 pazienti, 281 sono stati assegnati alla tripletta pomalidomide, bortezomib e desametasone e 278 al gruppo bortezomib e desametasone. Il follow-up mediano era di 15,9 mesi (range 9,9–21,7 mesi).
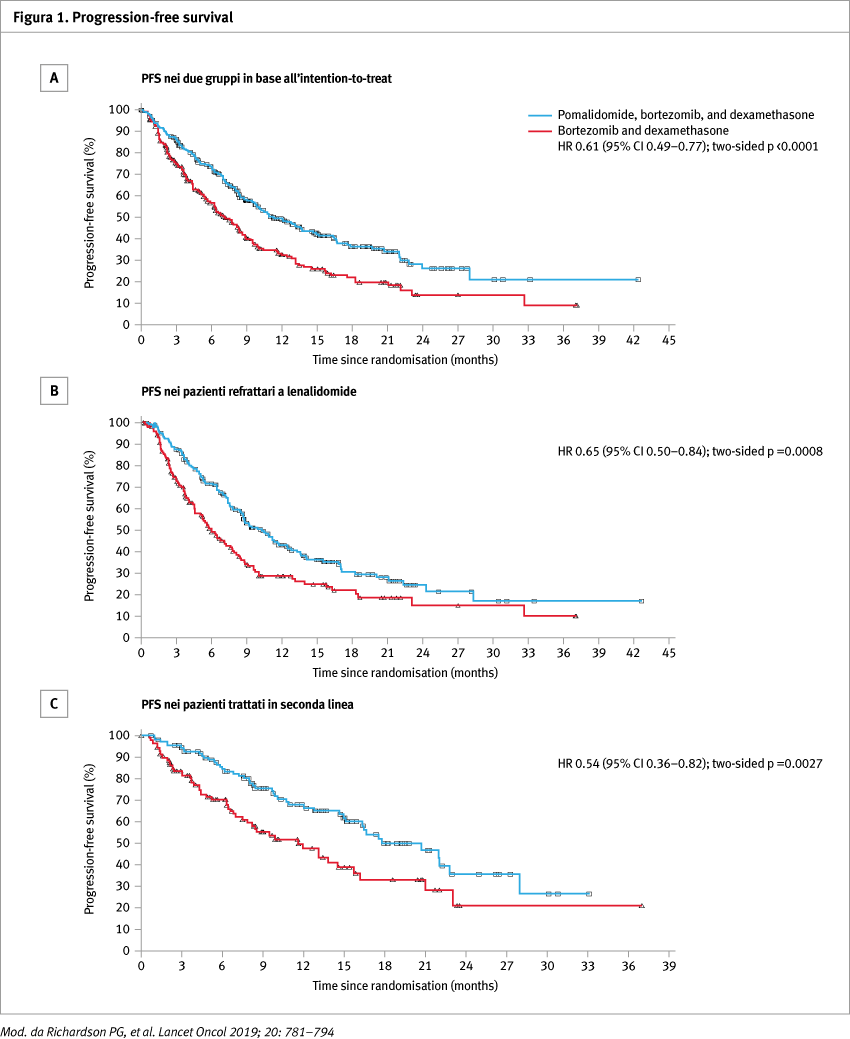
Nei pazienti trattati con la tripletta la PFS era significativamente incrementata rispetto al gruppo bortezomib-desametasone con una PFS mediana di 11,20 mesi (95% IC, 9,66–13,73) vs 7,10 mesi (5,88–8,48) con un hazard ratio di 0,61 (95% IC, 0,49–0,77; p <0,0001). 278 pazienti hanno ricevuto almeno una dose di pomalidomide, bortezomib e desametasone e 270 pazienti almeno una dose di bortezomib e desametasone, tutti questi pazienti sono stati considerati nell’analisi di valutazione della sicurezza.
L’aggiunta di pomalidomide ha comportato un incremento della neutropenia e del rischio infettivo:
- neutropenia (116 [42%] di 278 pazienti vs 23 [9%] di 270 pazienti) con 9 [3%] vs 0 pazienti con neutropenia febbrile)
- infezioni (86 [31%] vs 48 [18%]).
Tra gli eventi più comuni di grado 3 o 4 correlati al trattamento gli autori segnalano anche la piastrinopenia (76 [27%] vs 79 [29%]).
Per quanto riguarda gli eventi avversi seri sono stati osservati in 159 (57%) di 278 pazienti versus 114 (42%) di 270 del gruppo di controllo. Le morti correlate al trattamento sono state 8: 6 (2%) nel gruppo pomalidomide, bortezomib, desametasone (2 polmoniti, 2 decessi per causa non nota, 1 arresto cardiaco, 1 arresto cardiorespiratorio) e 2 eventi (1%) con bortezomib-desametasone (1 polmonite e 1 encefalopatia epatica).
Conclusioni
Nei pazienti con MM recidivati refrattari precedentemente esposti alla lenalidomide, l’aggiunta di pomalidomide alla terapia con bortezomib e desametasone conferisce un prolungamento significativo della PFS. Gli eventi avversi osservati nei due bracci di trattamento rispecchiano il profilo di tossicità dei singoli farmaci. L’incremento della PFS ottenuto con la tripletta nello studio OPTIMISMM sottolinea il potenziale di questa combinazione nei pazienti con MM recidivati refrattari precedentemente trattati con lenalidomide.