Numero speciale di "Impact Factor News” n° 4 - Ottobre 2020
Introduzione
Le cellule chimeriche del recettore dell'antigene T (CAR T) hanno mostrato un'attività drammatica in un piccolo numero di pazienti con leucemia linfatica cronica recidivata-refrattaria (CLL RR), con diversi pazienti ancora in remissione otto anni dopo l'infusione. In uno studio precedente gli sperimentatori hanno trattato 14 pazienti affetti da CLL RR con una mediana di 1,6x106 (range 0,14–11x106) cellule geneticamente modificate e hanno osservato un tasso di risposta globale (ORR) del 57%, comprese quattro risposte complete (CR) e quattro risposte parziali (PR). In quella piccola coorte non c'era evidente relazione tra dose e risposta o tossicità. Per determinare una dose cellulare ottimale per studi futuri, gli stessi autori hanno eseguito uno studio prospettico, randomizzato, di fase II, di due dosi di CAR T anti-CD19 (CAR T-19) in pazienti con CLL RR. Di seguito vengono riportati i risultati a lungo termine.
Metodi
Tra gennaio 2013 e giugno 2016 42 pazienti con CLL RR sono stati arruolati in questo studio e 38 sono stati reinfusi con cellule CAR T-19. Di questi, 28 pazienti sono stati inizialmente assegnati in modo casuale a ricevere una dose bassa (5×107) o alta (5×108) di CAR T-19 e, di questi, 24 pazienti erano valutabili per la valutazione della risposta. Dopo un'analisi ad interim, altri 10 pazienti hanno ricevuto la dose selezionata (alta) e, di questi, otto erano valutabili per la risposta. I pazienti sono stati seguiti per una mediana di 31,5 mesi (range 2–75).
Risultati
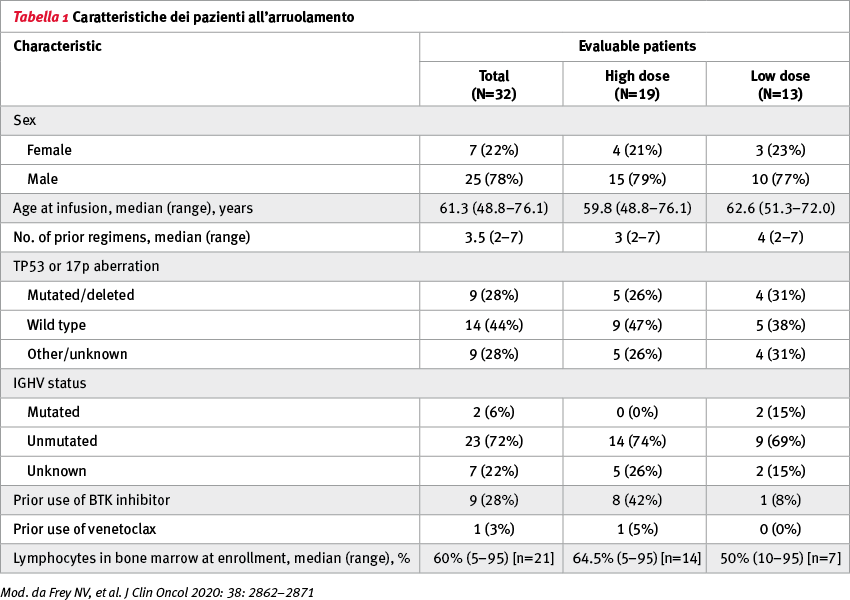
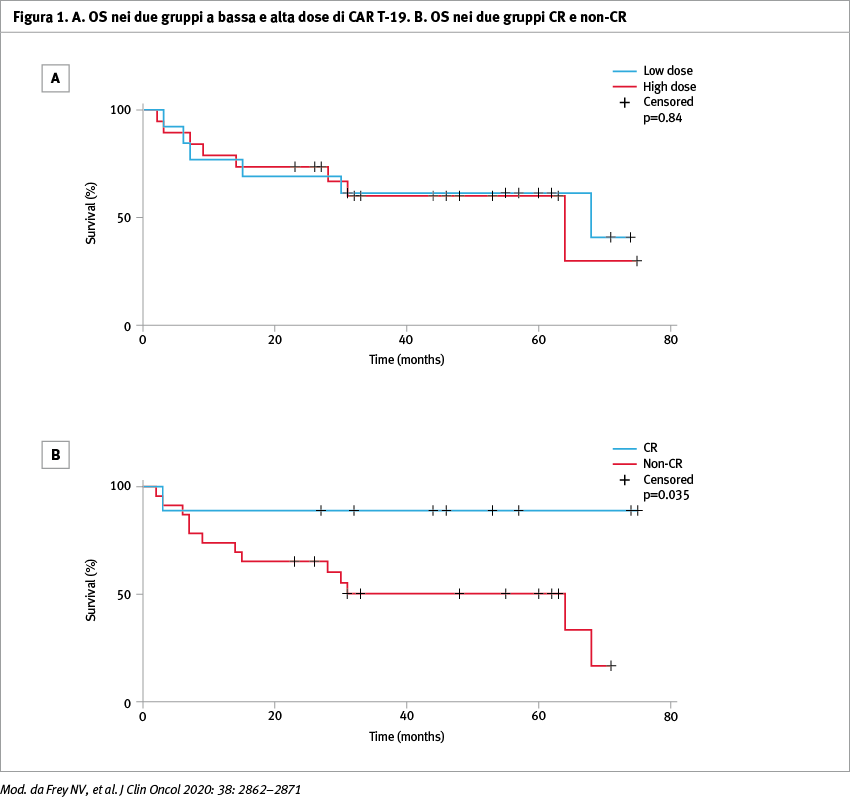
Le caratteristiche dei 32 pazienti arruolati sono riassunte nella Tabella 1. A quattro settimane le CR e OR per i 32 pazienti valutabili sono state rispettivamente del 28% (90% CI 16–44%) e del 44% (90% CI 29–60%). L’overall survival mediana (OS) per tutti i pazienti è stata di 64 mesi; non c'era alcuna differenza statisticamente significativa tra i gruppi a basso e ad alto dosaggio (p=0,84). Indipendentemente dalla dose, è stata osservata una sopravvivenza prolungata nei pazienti che hanno raggiunto una CR rispetto a quelli che non l'hanno raggiunta (p=0,035), con OS mediana non raggiunta nei pazienti con CR, rispetto a OS pari a 64 mesi in quelli senza CR (Figura 1). La progression-free survival (PFS) mediana è stata di 40,2 mesi nei pazienti con CR e di un mese in quelli senza CR (p <0,0001). La tossicità era comparabile in entrambi i gruppi di dosaggio.
Conclusioni
Gli autori concludono che un singolo ciclo di trattamento con CAR T-19 può indurre remissioni durevoli, con un profilo di tossicità accettabile in pazienti con CLL avanzata. Il raggiungimento di una CR dopo l'infusione di CAR T-19, indipendentemente dalla dose cellulare, è associato a una OS più lunga e alla PFS nel subset di pazienti con CLL in recidiva. Inoltre, una dose pari a 5×108 di CAR T-19 può essere più efficace di 5×107 CAR T-19 nell'indurre CR senza eccessiva tossicità.


