Numero speciale di "Impact Factor News” n° 4 - Ottobre 2023
Introduzione
Gli agenti stimolanti l’eritropoiesi (ESA) sono lo standard di trattamento dell’anemia nelle sindromi mielodisplastiche (MDS) a basso rischio ma la risposta è spesso transitoria. Luspatercept è un agente che promuove la maturazione eritroide attualmente indicato per il trattamento delle MDS trasfusione-dipendenti a basso rischio, con sideroblasti ad anello e in risposta insoddisfacente o non idonee alla terapia con eritropoietina (EPO). Lo studio COMMANDS, del quale sono stati recentemente pubblicati i risultati della valutazione ad interim sul New England Journal of Medicine, è il primo studio randomizzato che si propone di trovare un’alternativa terapeutica all’EPO nel management dell’anemia mediante il confronto diretto EPO vs luspatercept in una popolazione di pazienti con MDS trasfusione-dipendenti, non pretrattati, con o senza sideroblasti ad anello.
Metodi
Lo studio di fase III COMMANDS ha coinvolto 142 centri in 26 nazioni. Sono stati arruolati pazienti di età superiore ai 18 anni, con una diagnosi di MDS a rischio da molto basso a intermedio secondo i criteri del Revised-International Prognostic Scoring System (R-IPSS) e che avessero i seguenti requisiti: non pretrattati con ESA, trasfusione-dipendenti (2–6 unità di emazie concentrate/8 settimane, per almeno 8 settimane prima della randomizzazione) e con livelli di EPO inferiore a 500 U/L. I pazienti sono stati randomizzati con rapporto 1:1 a ricevere luspatercept sottocute una volta ogni 3 settimane (1 mg/kg, con possibilità di incremento fino a 1,75 mg/kg) o EPO alfa settimanale (a partire dal dosaggio di 450 UI/kg, incrementabile fino a 1050 UI/kg) per almeno 24 settimane. I pazienti sono stati stratificati in base al carico trasfusionale (inferiore o superiore a 4 unità/8 settimane), ai valori di EPO endogena (≤200 U/L vs >200 to <500 U/L) e alla presenza o assenza di sideroblasti ad anello. L’endpoint primario dello studio era il conseguimento dell’indipendenza trasfusionale (RBC-TI) per almeno 12 settimane con un concomitante incremento dei valori di emoglobina (Hb) pari o superiore a 1,5 g/dL. Tutti i pazienti che hanno ricevuto almeno una somministrazione del farmaco in studio sono stati inclusi nell’analisi di safety (ClinicalTrials.gov, NCT03682536).
Risultati
Un totale di 356 pazienti è stato randomizzato a ricevere luspatercept (178 pazienti) o EPO alfa (178 pazienti). L’età media era di 74 anni (69–80). La valutazione ad interim di efficacia è stata condotta sui 301 pazienti (luspatercept 147, EPO alfa 154) che avevano completato le 24 settimane di trattamento o che erano stati discontinuati dallo studio (durata mediana del trattamento di 41,6 e 27 settimane, rispettivamente). L’endpoint primario è stato raggiunto da 86/147 pazienti (59%) trattati con luspatercept e da 48/154 (31%) pazienti del gruppo EPO alfa (p <0,0001). I benefici del trattamento in termini di profondità e durata della risposta sono stati riscontrati anche nei sottogruppi clinicamente rilevanti. Nella Figura 1 si evidenzia come luspatercept abbia consentito di raggiungere degli endpoint secondari di indipendenza dal supporto trasfusionale per almeno 12 e 24 settimane e l’ottenimento di una risposta eritroide per 8 settimane in una percentuale di pazienti significativamente maggiore rispetto ad EPO.
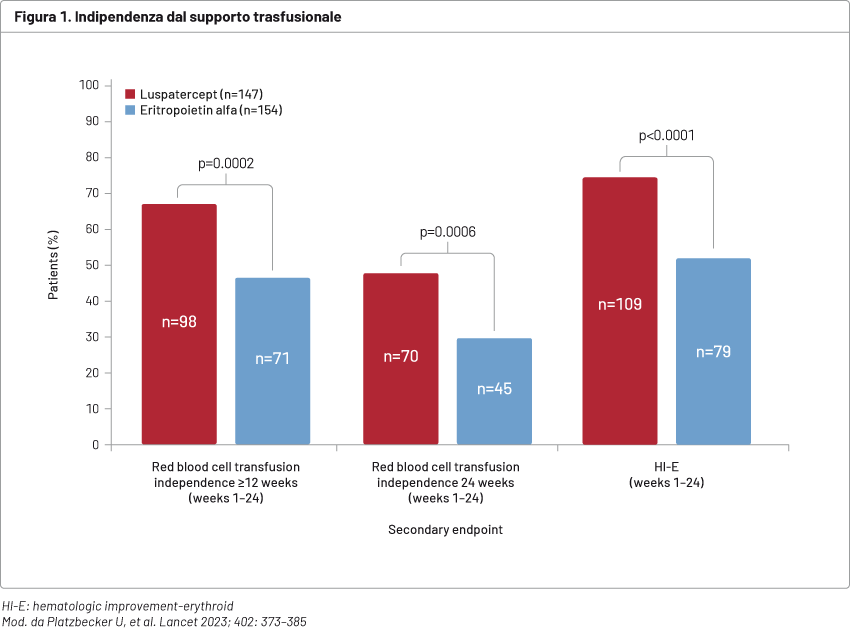
Per quanto riguarda la sicurezza del trattamento non si sono verificate tossicità inattese rispetto a quanto già noto per entrambi i farmaci.
Conclusioni
Gli autori concludono che, nei pazienti con MDS a basso rischio non pretrattata, luspatercept migliora il tasso di risposta in termini di indipendenza trasfusionale e incremento dei valori di Hb rispetto a EPO alfa. Benché sia necessario un follow-up più lungo e la conferma del risultato nei diversi sottogruppi, lo studio evidenzia come luspatercept potrebbe affermarsi in alternativa allo standard attuale di cura nei pazienti con o senza sideroblasti ad anello.


