Numero speciale di "Impact Factor News” n° 6 - Ottobre 2025
Introduzione
La terapia con cellule T con recettore dell’antigene chimerico (CAR-T) dirette contro CD19 è un'opzione terapeutica consolidata per il linfoma diffuso a grandi cellule B (DLBCL) recidivato/refrattario (R/R). Nonostante l'efficacia osservata con le CAR-T anti-CD19, circa la metà dei pazienti con DLBCL R/R recidiva, dopodiché la sopravvivenza globale (OS) mediana è di 5 mesi. Inoltre, molti pazienti non ricevono un trattamento successivo dopo le CAR-T, evidenziando un significativo bisogno medico insoddisfatto in questa popolazione.
Metodi
La coorte di espansione pre-specificata post-CAR-T dello studio ELM-1 ha valutato l'efficacia e la sicurezza di odronextamab, un anticorpo bispecifico CD20×CD3, in pazienti con progressione di malattia dopo CAR-T. Sessanta pazienti hanno ricevuto odronextamab per via endovenosa settimanalmente per 4 cicli, seguiti da mantenimento fino alla progressione. L'endpoint primario era il tasso di risposta obiettiva (ORR), valutato da un comitato di revisione indipendente (IRC). Questo studio è stato registrato su ClinicalTrials.gov (NCT02290951).
Risultati
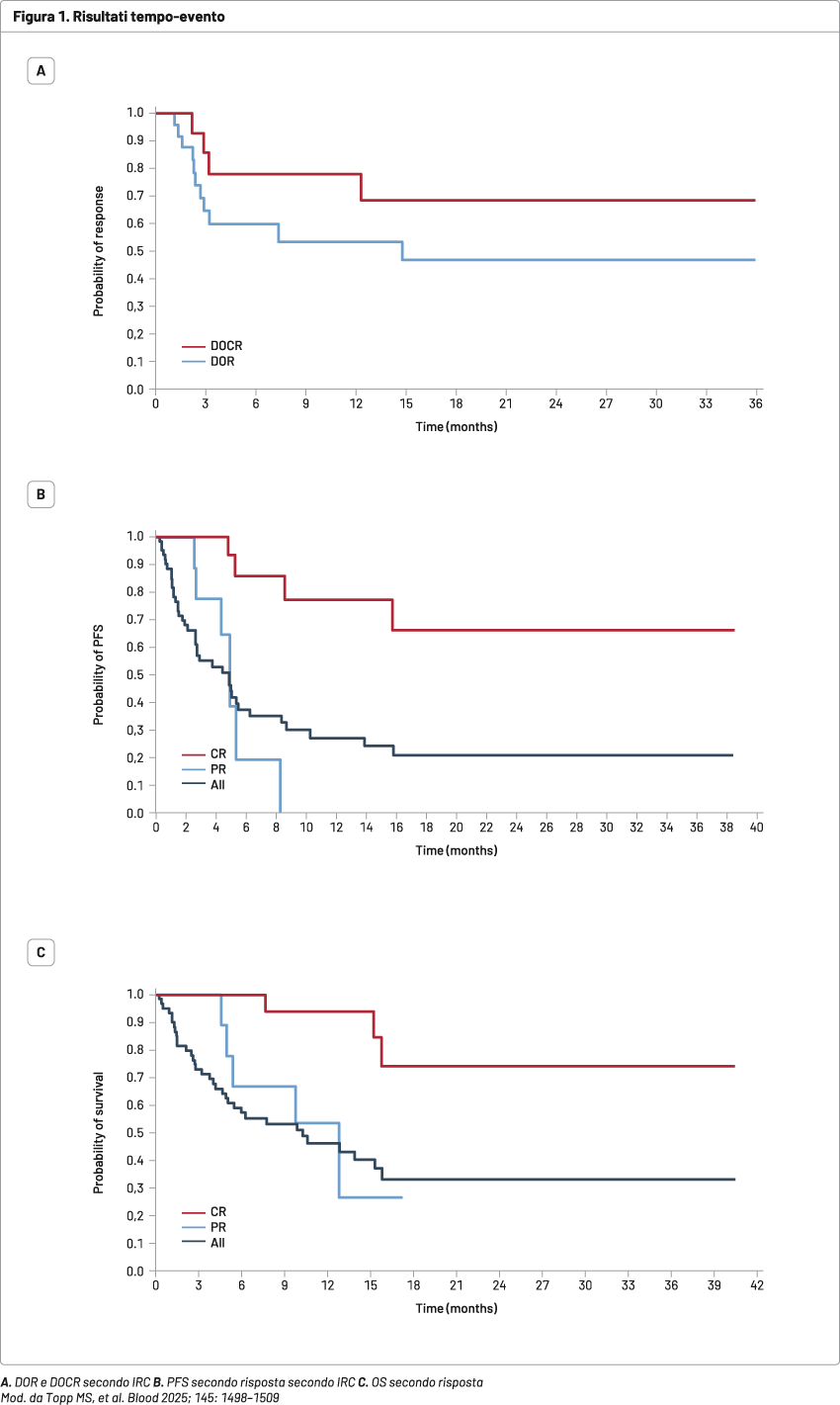
Il numero mediano di linee di terapia precedenti era 3 (intervallo 2–9), il 71,7% dei pazienti era refrattario alle CAR-T e il 48,3% aveva recidivato entro 90 giorni dalla terapia con CAR-T. Dopo un follow-up mediano di 16,2 mesi, l'ORR e il tasso di risposta completa (CR) erano del 48,3 e del 31,7%, rispettivamente. Le risposte erano simili tra i precedenti prodotti CAR-T e il tempo alla recidiva durante la terapia con CAR-T. La durata mediana della risposta era di 14,8 mesi e la durata mediana della CR non è stata raggiunta (Figura 1A). La sopravvivenza libera da progressione (PFS) e l’OS mediane erano di 4,8 e 10,2 mesi, rispettivamente (Figure 1B-C).
L'evento avverso più comune correlato al trattamento (TEAE) è stata la sindrome da rilascio di citochine (CRS) (48,3%; nessun evento di grado ≥3) (Tabella 1).
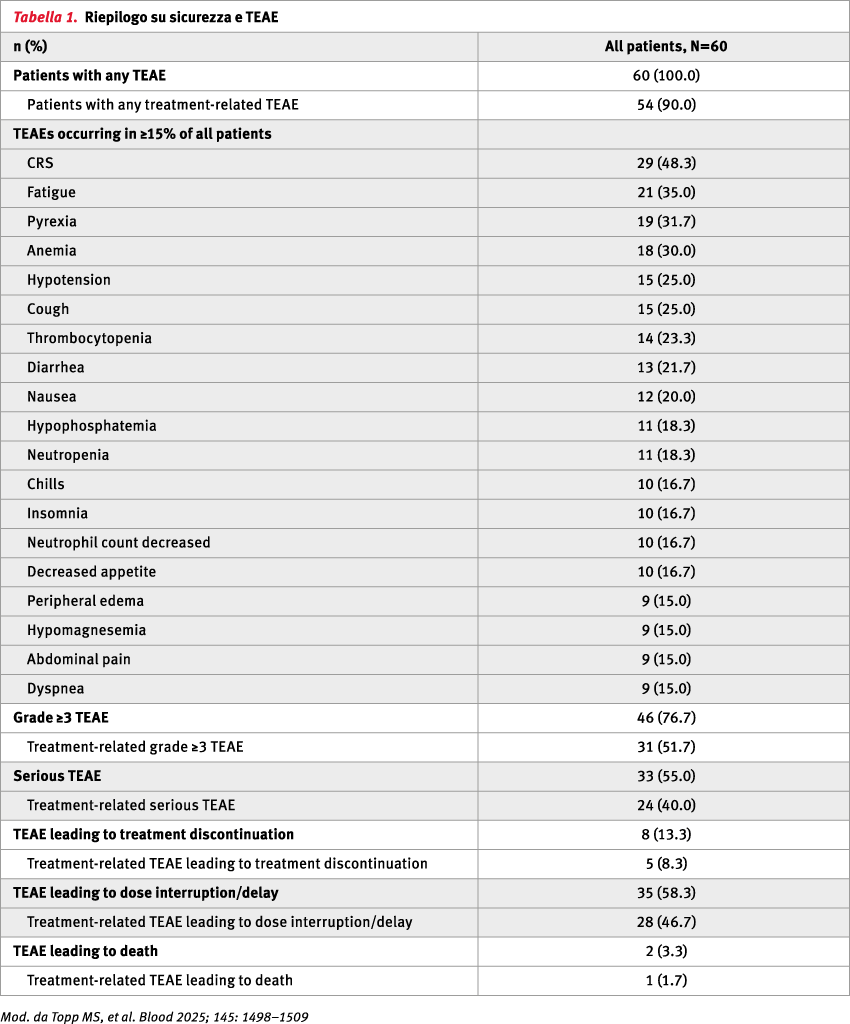
Non sono stati segnalati casi di sindrome da neurotossicità associata alle cellule effettrici immunitarie (ICANS). Infezioni di grado ≥3 si sono verificate in 12 pazienti (20,0%), 2 dei quali erano affetti da COVID-19.
Conclusioni
Gli autori concludono che odronextamab in monoterapia ha dimostrato un'efficacia incoraggiante e un profilo di sicurezza generalmente gestibile, supportando il suo potenziale come opzione standard per i pazienti che hanno fallito una terapia CAR-T. Nei pazienti con DLBCL in progressione dopo terapia con CAR-T, odronextamab ha mostrato un ORR del 48% e un tasso di CR del 32%. Odronextamab ha avuto un profilo di sicurezza generalmente gestibile, con il 48% di CRS di basso grado e il 20% di infezioni di grado ≥3.


