Numero speciale di "Impact Factor News” n° 1 - Aprile 2019
Introduzione
Nel mieloma multiplo di nuova diagnosi la somministrazione del mantenimento dopo il trapianto autologo (ASCT) può ritardare la progressione della malattia e prolungare la sopravvivenza. Dimopulos e coll. hanno presentato su Lancet i risultati dello studio TOURMALINE-MM3 nel quale ixazomib, inibitore delle proteasi con somministrazione orale settimanale e basso profilo di tossicità, è stato valutato in termini di sicurezza ed efficacia nel mantenimento dopo ASCT.
Metodi
Lo studio di fase 3, in doppio cieco, è stato condotto in 30 paesi in Europa, Medio Oriente, Africa, Asia e Nord e Sud America. I pazienti erano eleggibili in presenza dei seguenti requisiti: diagnosi confermata di mieloma multiplo sintomatico secondo i criteri dell’International Myeloma Working Group, risposta almeno parziale dopo un trattamento standard di induzione seguito da singolo ASCT, trapianto condizionato con melfalan 200 mg/m² ed eseguito entro 12 mesi dalla diagnosi. I pazienti sono stati randomizzati con rapporto 3:2 a ricevere ixazomib orale o placebo nei giorni 1, 8 e 15 in cicli di 28 giorni per due anni dopo l'induzione e l’ASCT. Il dosaggio iniziale di ixazomib di 3 mg era incrementato a 4 mg a partire dal quinto ciclo, in assenza di tossicità nei cicli precedenti. I pazienti venivano stratificati alla randomizzazione in base al regime di induzione ricevuto, allo stadio della malattia all’esordio e alla risposta post-trapianto. L'endpoint primario dello studio era la sopravvivenza libera da progressione (PFS). La sicurezza è stata valutata in tutti i pazienti che hanno ricevuto almeno una dose di ixazomib o placebo, in base al trattamento effettivamente ricevuto.
Risultati
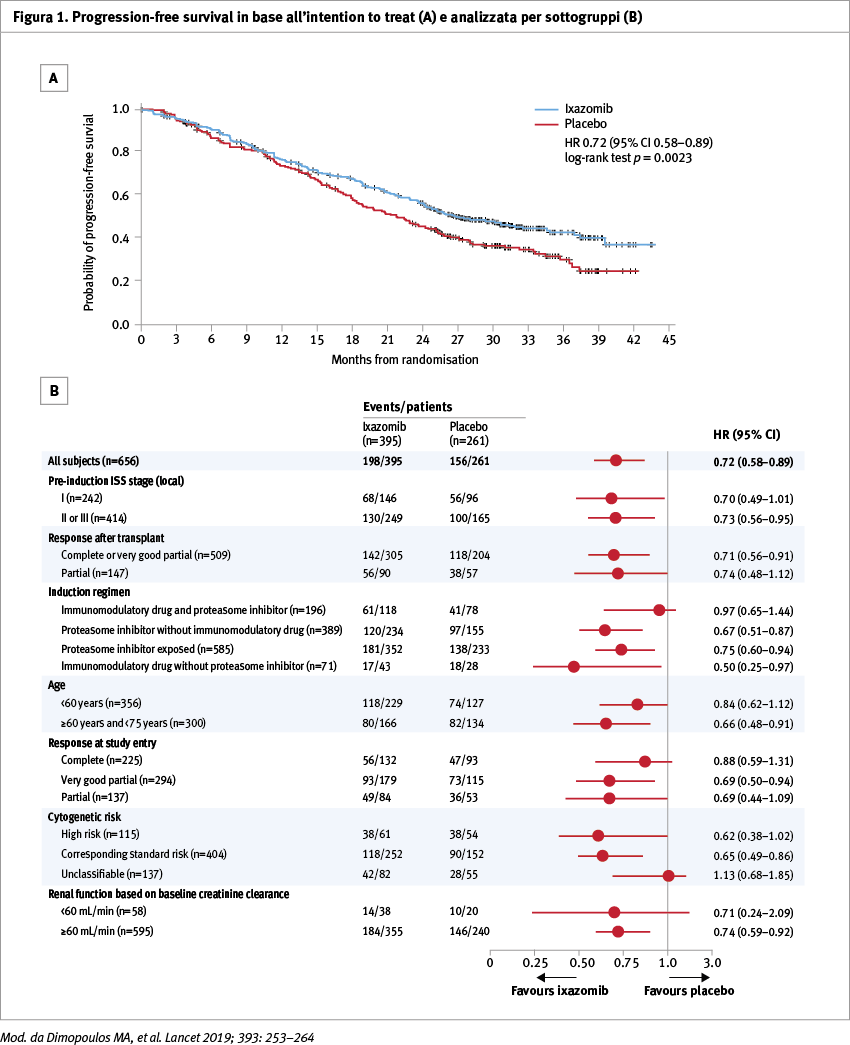
Tra il 31 luglio 2014 e il 14 marzo 2016, sono stati arruolati 656 pazienti, 395 nel braccio ixazomib e 261 nel braccio placebo. Con un follow-up mediano di 31 mesi, si è osservata una riduzione del rischio di progressione o morte del 28% con ixazomib rispetto al placebo (PFS mediana 26,5 mesi (95% CI 23,7–33,8) vs 21,3 mesi (18,0-24,7); HR 0,72, 95% CI, 0,58–0,89; p=0,0023) (Figura 1A). Il vantaggio era indipendente dalla pregressa esposizione a inibitori del proteosoma nella fase di induzione o dallo stato di malattia minima residua all’ingresso in studio. Il mantenimento con ixazomib determinava un miglioramento della prognosi anche nel sottogruppo di pazienti ad alto rischio citogenetico (PFS a 24 mesi 46% vs 24% con placebo) (Figura 1B).
Al momento dell’analisi oggetto di pubblicazione, non si era osservato un incremento dei secondi tumori nel gruppo ixazomib (12 pazienti, 3%) rispetto al placebo (8 pazienti, 3%).
L’incidenza degli eventi avversi seri è stata del 27% nel gruppo ixazomib e del 20% nel gruppo placebo. Durante il periodo di trattamento, si è verificato un solo decesso nel gruppo ixazomib.
Conclusioni
La somministrazione di ixazomib prolunga la PFS e rappresenta un'opzione aggiuntiva per la terapia di mantenimento post-trapianto in pazienti con mieloma multiplo di nuova diagnosi.
Nonostante non si possano confrontare i risultati ottenuti da studi clinic diversi, ixazomib somministrato per due anni sembrerebbe determinare un vantaggio minore in termini di PFS rispetto al mantenimento con lenalidomide, tuttavia ixazomib potrebbe rappresentare un’opzione per il mantenimento in caso di intolleranza alla lenalidomide o nella malattia ad alto rischio.