Numero speciale di "Impact Factor News" n° 3 - Aprile 2026
Introduzione
Nel contesto del linfoma follicolare (FL) recidivato o refrattario (R/R) persiste un bisogno insoddisfatto di regimi senza chemioterapia che inducano risposte durature. Lenalidomide e rituximab (R2) rappresentano uno standard di cura accettato in questa popolazione di pazienti. Lo studio EPCORE FL-1 mirava a valutare l'efficacia e la sicurezza di epcoritamab + R2 rispetto a R2 in pazienti con FL R/R dopo almeno una precedente linea di chemioimmunoterapia.
Metodi
In questo studio internazionale di fase 3, in aperto, i partecipanti sono stati assegnati in modo casuale (1:1) a ricevere epcoritamab a durata fissa + R2 o R2 per un massimo di 12 cicli. Epcoritamab è stato somministrato settimanalmente nei cicli 1–3 e ogni 4 settimane nei cicli 4–12, lenalidomide una volta al giorno durante i cicli 1–12 (giorni 1–21) e rituximab settimanalmente durante il ciclo 1 e mensilmente nei cicli 2–5. I due endpoints primari erano il tasso di risposta globale (ORR) e la sopravvivenza libera da progressione (PFS), valutati da un comitato di revisione indipendente. I dati qui riportati provengono da un'analisi ad interim pianificata, condotta dopo il verificarsi del 78% degli eventi di PFS. Questo studio è registrato su ClinicalTrials.gov (NCT05409066) ed EudraCT (2021-000169-34) ed è in corso (chiuso al reclutamento).
Risultati
Dei 668 partecipanti sottoposti a screening per l'idoneità in 189 centri accademici e non accademici in 30 paesi in Africa, Asia, Australia, Europa, Nord America e Sud America, un totale di 488 partecipanti sono stati assegnati in modo casuale: 243 a epcoritamab + R2 e 245 a R2. Lo studio ha raggiunto i suoi due endpoints primari, dimostrando la superiorità di epcoritamab + R2 rispetto a R2 in termini di ORR e PFS. Con un follow-up mediano di 14,8 mesi (interquartile range, IQR 11,4–19,0), l’ORR è stato del 95% (confidence interval, CI 95%: 92–97) con epcoritamab + R2 rispetto al 79% (74–84; p <0,0001) con R2. La PFS è stata più lunga con epcoritamab + R2 rispetto a R2 (hazard ratio, HR 0,21 [95% CI: 0,14–0,31], p <0,0001); la PFS stimata a 16 mesi ha favorito epcoritamab + R2 (85,5 vs 40,2%) (Figura 1).
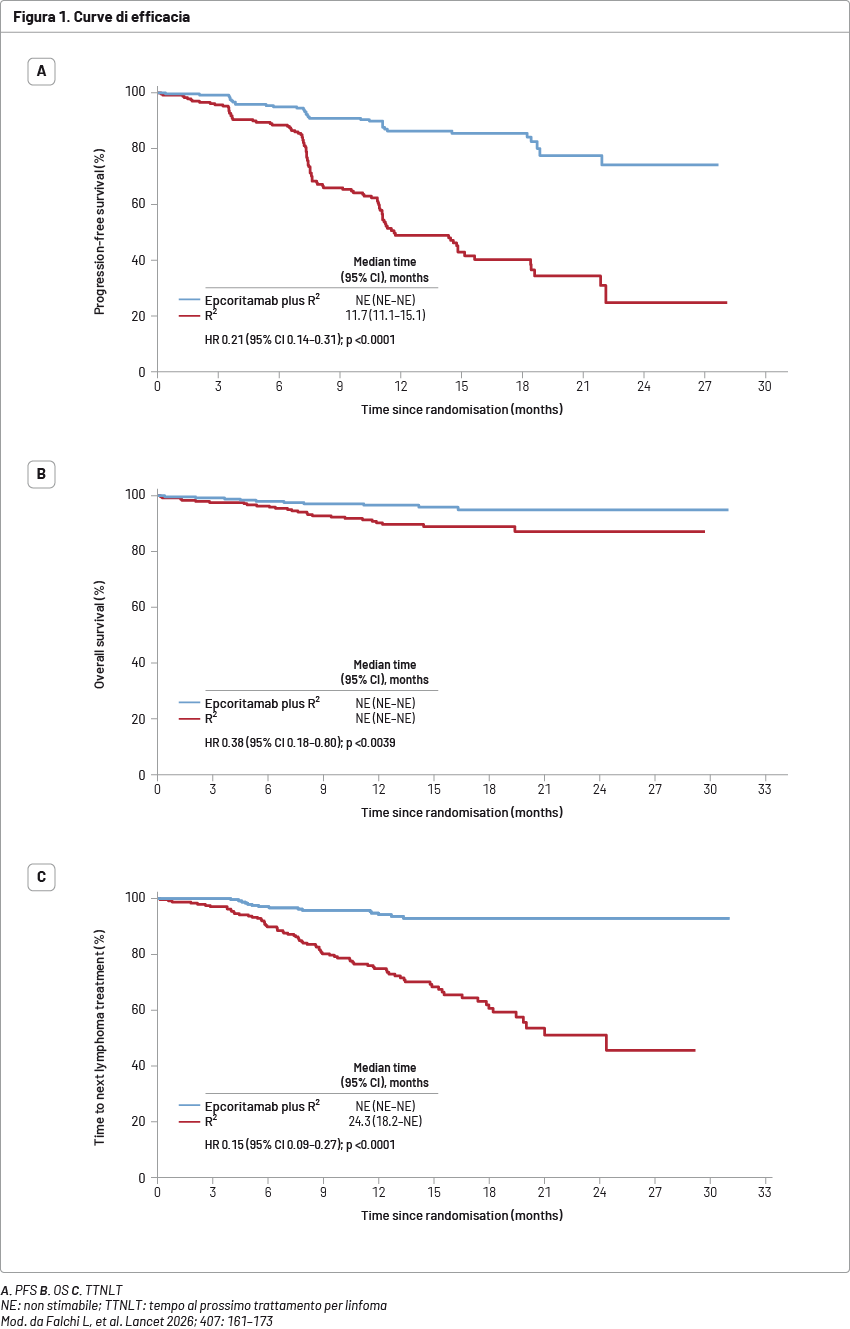
Eventi avversi (EA) di grado 3 o superiore sono stati più frequenti con epcoritamab + R2 (219 [90%] di 243 partecipanti) rispetto a R2 (161 [68%] di 238 partecipanti). La sindrome da rilascio di citochine è stata di basso grado con epcoritamab + R2 (grado 1 in 28 [21%] partecipanti e grado 2 in 7 [5%] partecipanti) e gestibile, e tutti gli eventi sono stati risolti.
Conclusioni
Epcoritamab + R2 ha determinato un tasso di risposta significativamente più elevato e una PFS più lunga rispetto a R2 tra i pazienti con FL che avevano ricevuto almeno una linea di terapia. Epcoritamab + R2 ha avuto più EA di grado 3 o superiore rispetto a R2. Gli EA sono stati gestibili e coerenti con i profili di sicurezza consolidati dei singoli componenti, senza l'identificazione di nuovi risultati di sicurezza. Questi risultati posizionano epcoritamab + R2 come un nuovo standard di cura per il trattamento del FL in seconda linea o successiva.


