Numero speciale di "Impact Factor News” n° 4 - Ottobre 2016
Background
L’immunochemioterapia secondo schema fludarabina, ciclofosfamide e rituximab (FC-R) è considerata il gold standard per i pazienti affetti da BLLC fit e malattia avanzata. In questo studio internazionale di fase III gli Autori hanno voluto testare un nuovo schema meno tossico per verificare se in termini di efficacia possa essere paragonato a FC-R.
Pazienti e metodi
Nello studio sono stati inclusi pazienti in prima linea di trattamento con età compresa tra i 33 e gli 81 anni, senza la del(17p) le cui caratteristiche di malattia sono state revisionate attraverso una valutazione centralizzata. I pazienti sono stati randomizzati attraverso una assegnazione 1:1 generata da un processore computerizzato e sono stati stratificati secondo i paesi di provenienza e lo stadio di Binet. I pazienti venivano assegnati rispettivamente a ricevere lo schema FC-R ev: fludarabina (25 mg/m²/die) ciclofosfamide (250 mg/m² /die) per i primi 3 giorni o bendamustina (90 mg/m² /die) per i primi 2 giorni di ogni ciclo. Rituximab veniva somministrato alla dose di 375 mg/m² in entrambi i gruppi al giorno 0 del primo ciclo e successivamente alla dose di 500 mg/m² al giorno 1 dei successivi 5 cicli. L’obiettivo primario dello studio era la PFS, con l’obiettivo principale di stabilire la non inferiorità di bendamustina-rituximab verso lo standard di trattamento dato da FC-R. Gli Autori hanno dichiarato che volevano dimostrare che la progression-free survival (PFS) di bendamustina-rituximab non doveva essere del 67,5% o meno per decretare la non inferiorità che corrisponde a un margine di non inferiorità pari a 1,388 della hazard ratio (HR) basata su un IC del 90,4%. L’analisi finale è stata fatta su un programma di intention to treat (ITT). Lo studio è stato registrato su ClinicalTrials.gov, numero NCT 00769522.
Risultati
Tra ottobre 2008 e luglio 2001 sono stati arruolati 688 pazienti, di questi 564 rispettavano i criteri di inclusioni previsti dallo studio e quindi sono stati randomizzati nei due bracci del trial. Di questi ultimi, 561 sono stati considerati nella popolazione di analisi per ITT: 282 pazienti nel braccio FC-R (gruppo A) e 279 nel braccio bendamustina-rituximab (gruppo B). Dopo una mediana di osservazione di 37,1 mesi (IQR 31,0–45,5) la PFS mediana era di 41,7 mesi (95% CI 34,9–45,3) nel gruppo B e 55,2 mesi (95% CI non calcolabile) nel gruppo A (HR 1,643, 90,4% CI 1,308–2,064). Il limite superiore dell’ICA di 90,4% CI era maggiore di 1,388, quindi l’ipotesi di non inferiorità dello schema bendamustina-rituximab veniva invalidata. Per quanto riguarda il profilo di tossicità registrato durante lo studio, la neutropenia severa e le infezioni sono state significativamente più numerose nel gruppo A rispetto al gruppo B (235 [84%] su 279 vs 164 [59%] su 278 e 109 [39%] vs 69 [25%], rispettivamente). L’incremento della frequenza delle complicanze infettive nel gruppo A era significativamente superiore nei pazienti con età >65 anni.
Conclusioni
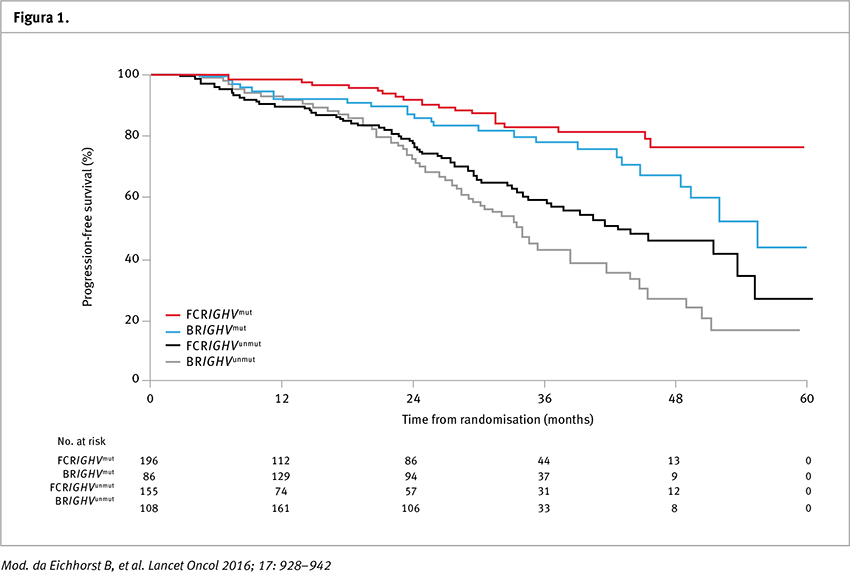
Gli Autori concludono che lo schema FC-R rimane lo standard di prima linea per pazienti affetti da BLLC, non solo, nel subset di pazienti con IGVH- mutate (Figura 1), lo schema sembra avere un potenziale di guarigione dalla malattia, visto il lungo follow-up e il raggiungimento di un plateau della curva di sopravvivenza. Bendamustina-rituximab è associato a un minor numero di eventi avversi nei pazienti con età superiore a 65 anni, pertanto in questo subset di pazienti lo schema può essere considerato una valida alternativa che controbilancia la minor efficacia.