Numero speciale di "Impact Factor News” n° 4 - Ottobre 2023
Introduzione
Ciltacabtagene autoleucel (cilta-cel) è una terapia con cellule T con recettore dell’antigene chimerico (CAR-T) in grado di riconoscere e legare l’antigene di maturazione delle cellule B (BCMA), presente sulle cellule del mieloma, ed è efficace nei pazienti con mieloma multiplo (MM) recidivato o refrattario (R/R) pesantemente pretrattati. Lo studio multicentrico internazionale CARTITUDE-4 ha valutato l’efficacia di cilta-cel in pazienti con MM refrattario alla lenalidomide in linee precoci di trattamento e ne ha dimostrato la capacità di ridurre il rischio di progressione o morte del 74% rispetto alla terapia standard (SOC).
Metodi
In questo studio di fase III, randomizzato, in aperto, i pazienti con MM refrattario a lenalidomide trattati in precedenza con non più di tre linee di terapia sono stati trattati con una somministrazione di cilta-cel o una terapia standard a scelta tra pomalidomide-bortezomib-desametasone (PVd) o daratumumab-pomalidomide- desametasone (DPd). L’outcome primario era la sopravvivenza libera da progressione (PFS). Gli endpoints secondari includevano altri parametri di valutazione della risposta, la safety e gli outcomes riportati dal paziente.
Risultati
Un totale di 419 pazienti (età mediana 61,5 anni) sono stati randomizzati con rapporto 1:1 (208 a ricevere cilta-cel e 211 a ricevere SOC). Con un follow-up di 15,9 mesi (0,1–27,3), lo studio CARTITUDE-4 ha soddisfatto l’endpoint primario di efficacia: la PFS mediana non è stata raggiunta nel gruppo cilta-cel ed è stata di 11,8 mesi con la SOC (hazard ratio, HR 0,26; confidence interval CI 95%: 0,18–0,38; p <0,001) (Figura 1).
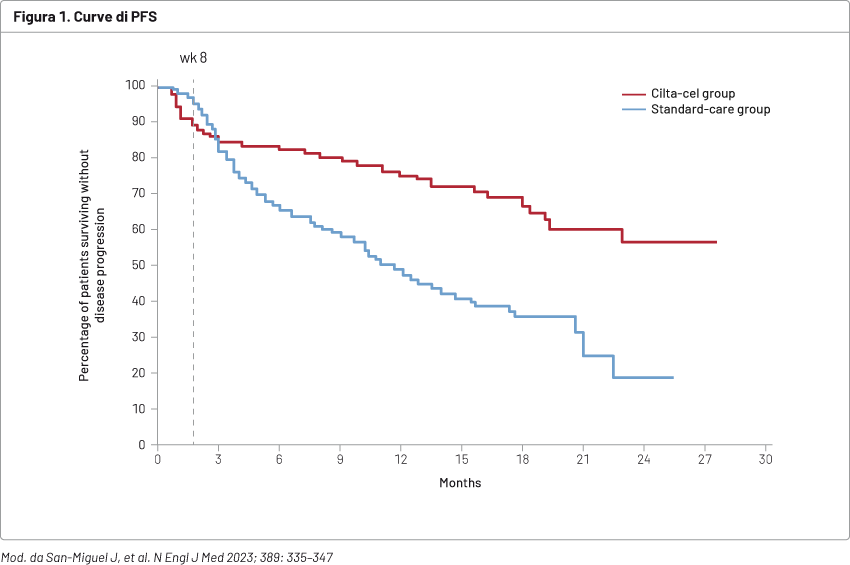
La PFS a 12 mesi è stata del 75,9% con le CAR-T e del 48,6% con la SOC. Per quanto riguarda i tassi di risposta, un maggior numero di pazienti trattati con cilta-cel ha ottenuto una risposta complessiva (84,6 contro 67,3%), una risposta completa o migliore (73,1 vs 21,8%) e la negativizzazione della malattia minima residua (MRD) (60,6 contro 15,6%). Per quanto riguarda la sicurezza, si sono verificati eventi avversi di grado 3 o 4 nella maggior parte dei pazienti arruolati (97 e 94%, rispettivamente, con cilta-cel e SOC), incluse infezioni (27 e 25%) e citopenie (94 e 86%). Tra i 176 pazienti che hanno ricevuto cilta-cel, l’incidenza della sindrome da rilascio di citochine (CRS) è stata del 76,1% (grado 3 o 4, 1,1%; grado 5, nessuno), l’incidenza di sindrome da neurotossicità associata alle cellule immunitarie effettrici (ICANS) è stata del 4,5% (tutti eventi G1 o G2), un paziente ha manifestato problemi motori e neurocognitivi G1, il 9,1% ha avuto paralisi dei nervi cranici (G2, 8%; G3, 1,1%) e il 2,8% ha avuto neuropatia periferica correlata a CAR-T (G1 o 2, 2,3%; grado 3, 0,6%). Nel complesso, si sono verificati 39 decessi nel braccio cilta-cel e 46 decessi in quello SOC (HR 0,78; CI 95%: 0,5–1,2); di questi, 10 e 5, rispettivamente, sono stati indotti da eventi avversi correlati al trattamento.
Conclusioni
Una singola infusione di cilta-cel è in grado di determinare risposte rapide e profonde con una riduzione del rischio di progressione o di morte rispetto alle cure standard nei pazienti affetti da MM refrattari a lenalidomide trattati con 1-3 linee di terapia. I brillanti risultati ottenuti mettono in luce le potenzialità di cilta-cel come possibile alternativa terapeutica per i mielomi dopo la prima recidiva (CARTITUDE-4, NCT04181827).


