Numero speciale di "Impact Factor News” n° 6 - Ottobre 2025
Introduzione
I pazienti con mieloma multiplo (MM) spesso recidivano dopo una terapia di prima linea con tripletta o quadrupletta, inclusi inibitori del proteasoma, agenti immunomodulatori e anticorpi monoclonali anti-CD38, evidenziando la necessità di combinazioni di trattamento di seconda linea efficaci che includano terapie con nuovi meccanismi d'azione. L’antigene BCMA è consolidato nel trattamento del MM e belantamab mafodotin, anticorpo coniugato anti-BCMA, aveva già mostrato attività clinica promettente come agente singolo (DREAMM-1 e -2) e azione sinergica in combinazione con altri farmaci. Belantamab mafodotin è stato associato a bortezomib e desametasone (BVd) e confrontato con daratumumab, bortezomib e desametasone (DVd) nello studio DREAMM-7; inoltre, è stato associato a pomalidomide e desametasone e confrontato con pomalidomide, bortezomib e desametasone nello studio DREAMM-8 (NCT04484623). Nelle analisi primarie, DREAMM-7 e DREAMM-8 hanno mostrato un beneficio significativo in termini di sopravvivenza libera da progressione (PFS) e trend positivi iniziali per la sopravvivenza globale (OS) a favore delle combinazioni di belantamab mafodotin rispetto ai rispettivi comparatori, con follow-up in corso. Su Lancet Oncology è stata recentemente pubblicata l’analisi aggiornata dello studio DREAMM-7, comprendente i dati di OS con follow-up di 39,4 mesi.
Metodi
DREAMM-7 è uno studio di fase 3, randomizzato, open-label, multicentrico (142 centri, 20 Paesi) che ha arruolato 494 pazienti adulti (età mediana 64,5 anni) con MM recidivato/refrattario (R/R) dopo ≥1 linea di terapia. I pazienti hanno ricevuto il seguente trattamento: nel braccio sperimentale BVd, belantamab 2,5 mg/kg endovena (ev) ogni 3 settimane + bortezomib sottocutaneo (sc) + desametasone; nel braccio standard DVd, daratumumab ev + bortezomib sc + desametasone. L’endpoint primario dello studio era la PFS. Gli endpoints secondari comprendevano la valutazione dell’OS, il tasso di negatività della malattia residua misurabile (MRD), la durata della risposta e la sicurezza.
Risultati
Con un follow-up mediano di 39,4 mesi, sono stati osservati i seguenti risultati: in termini di OS, si è rilevato un vantaggio di sopravvivenza nel braccio BVd rispetto a DVd, con un hazard ratio (HR) 0,58, p=0,0002, riduzione del 42 % del rischio di morte (OS mediana non raggiunta in entrambi i bracci) (Figura 1).
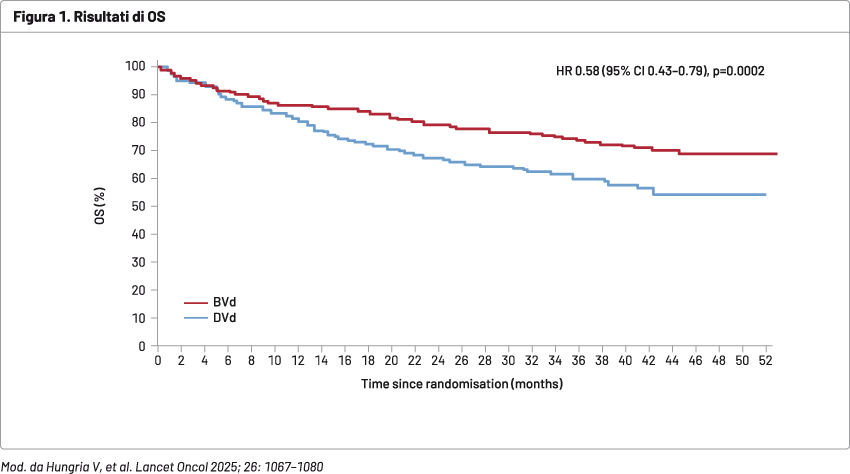
Inoltre, la MRD-negatività (nei pazienti in risposta completa [CR] o migliore) è stata pari al 25% con BVd vs 10% con DVd; la durata mediana della risposta è stata pari al 40,8 vs 17,8 mesi; per la PFS2 (dopo terapia successiva) è stato mantenuto il vantaggio nel braccio sperimentale, con una PFS2 mediana non raggiunta con BVd versus 33,4 mesi con DVd (HR 0,59) (Figura 2).
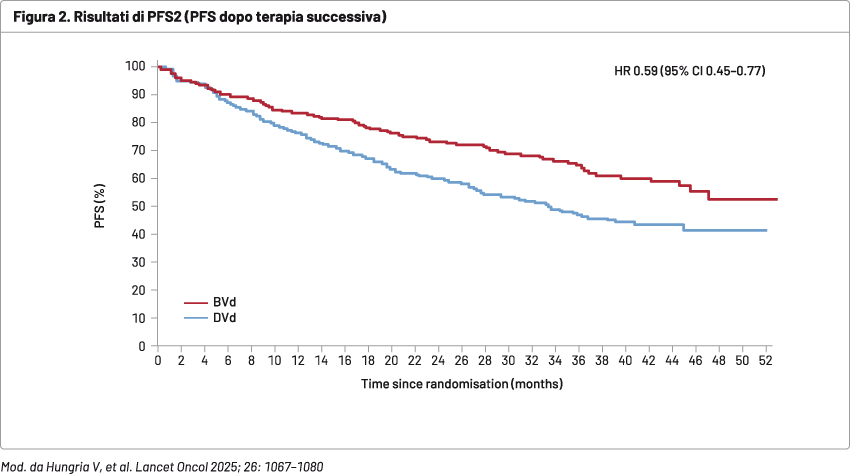
Per quanto riguarda la tossicità, gli eventi di grado ≥3 sono stati più frequenti con BVd (56 vs 35%). L’evento avverso più comune G3-G4 è stato la trombocitopenia (BVd 56% vs DVd 35%). Gli eventi oculari, un rischio noto con belantamab mafodotin, sono stati gestiti efficacemente con modifiche della dose e generalmente sono stati reversibili con un follow-up adeguato, consentendo ai pazienti di proseguire il trattamento e continuare a trarne beneficio. I decessi correlati al trattamento sono stati del 3% BVd vs 1% DVd.
Conclusioni
DREAMM-7 ha dimostrato un vantaggio significativo in OS e PFS di BVd rispetto a DVd. I pazienti trattati con BVd hanno ottenuto risposte più profonde e durature, con MRD-negatività doppia rispetto a DVd. Considerato l’esteso uso di daratumumab in prima linea, sia nei pazienti eleggibili sia nei non eleggibili a trapianto, con conseguente refrattarietà di molti pazienti all’anti-CD38 dopo la prima linea, BVd emerge come un’efficace opzione anti-BCMA-based e anti-CD38-free nella seconda linea nel MM R/R.


