Numero speciale di "Impact Factor News” n° 6 - Ottobre 2025
Introduzione
La terapia con cellule T con recettore dell’antigene chimerico (CAR-T) dirette contro CD19 ha trasformato il trattamento dei tumori a cellule B. Attualmente, quattro prodotti a base di cellule CAR-T anti-CD19 di seconda generazione sono disponibili in commercio e approvati per il trattamento di diversi linfomi a cellule B. Queste terapie incorporano un dominio co-stimolatorio intracellulare 4-1BB (CD137) o un dominio co-stimolatorio CD28 per migliorare l'attivazione e la persistenza delle cellule T. Nonostante questi progressi, oltre il 50% dei pazienti con linfoma non ottiene una remissione a lungo termine con la terapia con cellule CAR-T anti-CD19. Questi pazienti hanno opzioni terapeutiche limitate e una prognosi sfavorevole. Una strategia promettente per migliorare l'efficacia delle cellule CAR-T consiste nello sviluppo di cellule CAR-T ingegnerizzate di quarta generazione che secernono citochine proinfiammatorie per rafforzare l'attività antitumorale. In questo lavoro, gli sperimentatori hanno progettato un prodotto cellulare CAR-T potenziato (corazzato) anti-CD19 (huCART19-IL18) che secerne interleuchina-18 per potenziare l'attività antitumorale.
Metodi
Si tratta di uno studio di fase 1 monocentrico, che ha come obiettivo primario quello di valutare la sicurezza e, secondariamente, la fattibilità e l'efficacia preliminari di huCART19-IL18 in pazienti con linfoma recidivato/refrattario (R/R) dopo precedente terapia con cellule CAR-T anti-CD19. Utilizzando un processo di produzione di tre giorni, sono state somministrate cellule huCART19-IL18-positive in dosi comprese tra 3×106 e 3×108. Lo studio è stato registrato su ClinicalTrials.gov (NCT04684563).
Risultati
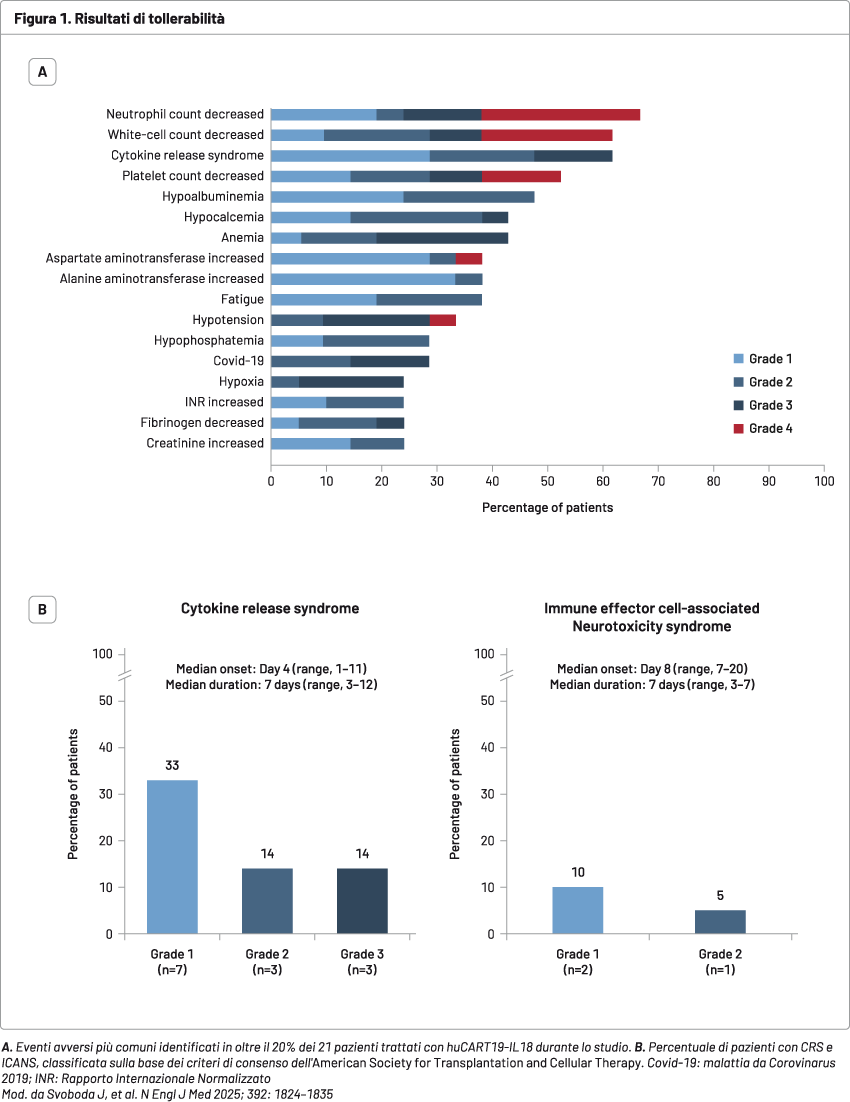
Un totale di 21 pazienti ha ricevuto huCART19-IL18. La sindrome da rilascio di citochine (CRS) si è verificata nel 62% dei pazienti (47% di grado 1 o 2) e la sindrome da neurotossicità associata alle cellule effettrici immunitarie (ICANS) si è verificata nel 14% dei pazienti (tutti di grado 1 o 2). Non sono stati osservati eventi avversi inattesi (Figura 1).
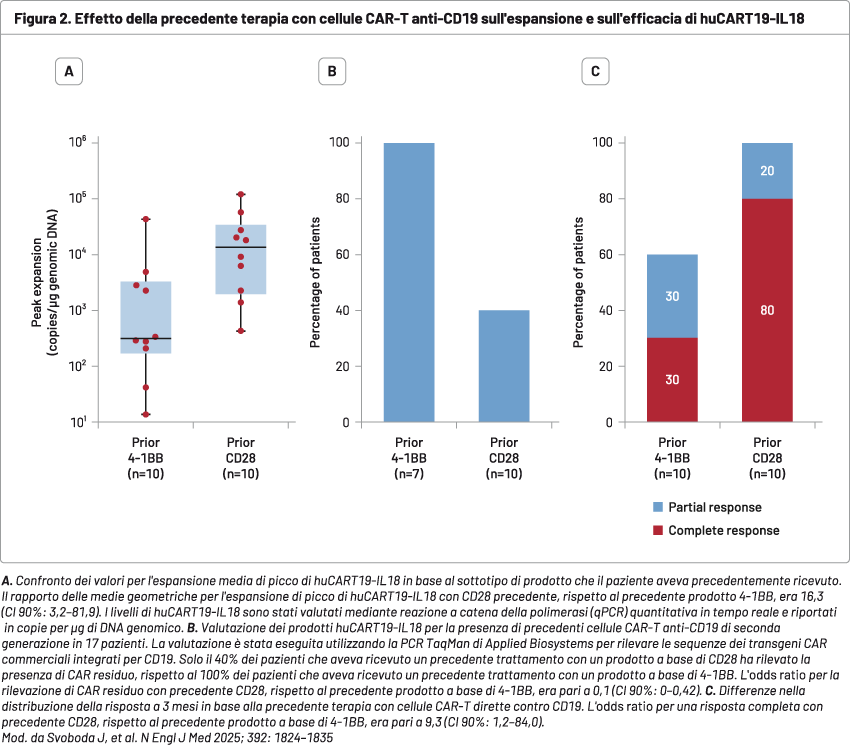
È stata rilevata una robusta espansione delle cellule CAR-T a tutti i livelli di dose (Figura 2).
A tre mesi dall'infusione, è stata osservata una risposta completa (CR) o parziale (PR) nell'81% dei pazienti (confidence interval, CI 90%: 62–93) e una CR nel 52% (CI 90%: 33–71) (Figura 3).
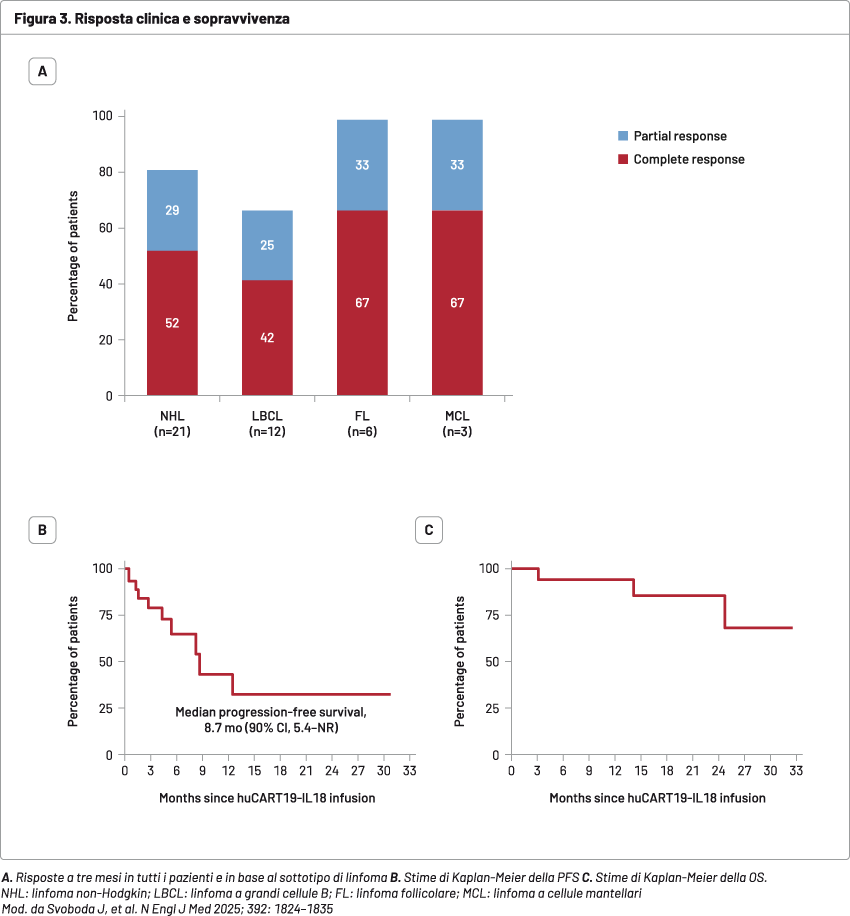
Con un follow-up mediano di 17,5 mesi (intervallo 3–34), la durata mediana della risposta è stata di 9,6 mesi (CI 90%: 5,5– non raggiunta).
Conclusioni
In questo piccolo studio, huCART19-IL18 ha mostrato un profilo di sicurezza coerente con altri trattamenti con cellule CAR-T e ha dimostrato un'efficacia promettente a basse dosi cellulari in pazienti con linfoma dopo il fallimento della precedente terapia con cellule CAR-T anti-CD19.


